
【题目】在一定温度下的定容容器中,当下列的物理量不再发生变化时,表明反应A(s)+2B(g)C(g)+D(g)已达到平衡状态的是( )
A.混合气体的压强不变
B.v(A):v(B)=1:2
C.B物质的量不变
D.c(B)=c(D)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】草酸晶体(H2C2O42H2O)无色,易溶于水,熔点为101℃(失水后能升华),170℃以上分解。其钠、钾、铵盐均易溶于水,而钙盐难溶于水。某实验探究小组对草酸晶体进行加热,并验证其分解产物。
(1)加热草酸晶体最适宜选用下图中的_______(填装置编号),不选其它装置的原因是 _________。
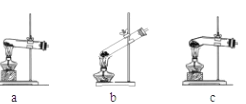
(2)若将产生的气体直接通入澄清石灰水来检验分解产物中是否含CO2,请你评价正确与否并作简要的解释___________。
(3)用下图装置检验草酸的分解产物H2O(g)、CO2和CO.将这种混合气体依次通过___________(填装置中接口的字母,可重复使用)。
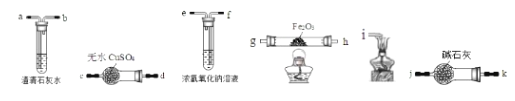
(4)能否依据硬质玻璃管Fe2O3质量的减轻来计算分解产生CO的量?_____。假设硬质玻璃管中所装为铁氧化物的混合物,可能是FeO、Fe2O3、Fe3O4的任意组合,现取ag混合物充分反应后,质量减轻了8a/29克,通过计算确定该混合物中三种氧化物的物质的量的关系为____。
(5)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_______。
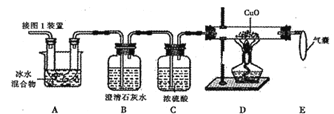
(6)有同学设计下图装置来证明Fe2O3反应后的固体中含有单质铁,你认为可行吗?____,其原因是:_______;图中安全漏斗的作用是____________________。
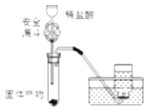
(7)设计一个简单的实验证明草酸是弱酸:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三周期元素X、Y、Z、W的最高价氧化物溶于水可得四种溶液,0.010mol/L的这四种溶液pH与该元素原子半径的关系如下图所示。下列说法正确的是

A. 简单离子半径:X>Y>Z>W
B. Z元素形成的单质存在同素异形体
C. 气态氢化物的稳定性:Z>W>Y
D. X和Y的最高价氧化物对应的水化物恰好中和时,溶液呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应4A+2B![]() 3C,下列说法中正确的是
3C,下列说法中正确的是
A. 某温度时,化学反应速率无论用A. B. C中任何物质表示,其数值都相同
B. 其他条件不变时,降低温度,化学反应速率减小
C. 其他条件不变时,增大压强,化学反应速率一定加快
D. 若增大或减小A的物质的量,化学反应速率一定会发生明显的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. 加入催化剂有利于氨的合成
D. 新制的氯水在光照条件下颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,他们进行了如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入下图所示的蒸馏烧瓶中(夹持和加热仪器略去),然后逐滴加入足量10%NaOH溶液,加热烧瓶将氨蒸出,用V1mLc1mol·L-1的盐酸吸收蒸出的氨,然后取下锥形瓶,用c2 mol·L-1 NaOH标准溶液滴定过剩的HCl。.终点时消耗V2 mLNaOH溶液。

②氯的测定:准确称取样品X配成溶液,用K2CrO4溶液为指示剂,用AgNO3标准溶液滴定,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)
回答下列问题:
(1)X的制备过程中,温度不能过高,其原因是____________________________
(2)仪器a的名称是________________;测定氨前应该对装置进行气密性检验,若气密性不好则测定结果将________(填“偏高”或“偏低”).该滴定过程中选择________做指示剂。
(3)样品中氨的质量分数表达式为_____________________________。
(4)测定氯的过程中,AgNO3标准溶液置于_________(填“无色”或“棕色”)滴定管中;滴定终点时,溶液中已检测不到Cl-[c(Cl-)≤1.0×10-5 mol·L-1],则出现砖红色沉淀时,溶液中c(CrO42-)的最小值为_____________mol·L-1。[已.知:Ksp(AgCl)=1.0×10-10,Ksp( Ag2CrO4)=1.12×10-12]
(5)经测定分析,样品X中钴、氨和氯的物质的量之比为1:6:3,则制备X的化学方程式为________________________________________。
(6)某同学向CoCl2溶液中加入足量(NH4)2C2O4得到CoC2O4沉淀,在空气中煅烧CoC2O4生成钻氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则所得钴氧化物的化学式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成如图所示的原电池,下列叙述正确的是

A. KNO3盐桥中的K+移向CuSO4溶液
B. Ag作负极,Cu作正极
C. 工作一段时间后,CuSO4溶液中c(Cu2+)增大
D. 取出盐桥后,电流计的指针依然发生偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)烧杯间填满碎纸条的作用是____________________。
(2)大烧杯上如不盖硬纸板,求得的中和热的数值_________(填“偏大”“偏小”“无影响”)。
(3)从实验装置上看,图中如果没有环形玻璃搅拌棒搅拌,如此求得的中和热的数值_________(填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量_____________________(填“相等”“不相等”),所求中和热____________(填“相等”“不相等”),简述理由:_______________________________。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会______________;用50 mL 0.50 mol·L-1NaOH溶液进行上述实验,测得的中和热的数值会_____________________。(均填“偏大”“偏小”“无影响”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com