
NH4Al(SO4)2��ʳƷ�ӹ�����Ϊ��ݵ�ʳƷ���Ӽ������ڱ���ʳƷ��NH4HSO4�ڷ����Լ���ҽҩ�����ӹ�ҵ����;�㷺����ش��������⣺
(1)NH4Al(SO4)2������ˮ������ԭ����____________________(�����ӷ���ʽ˵��)��
(2)��ͬ�����£�0.1 mol��L��1 NH4Al(SO4)2 ��Һ�� c(NH4+)________(����ڡ��������ڡ���С�ڡ�)0.1 mol��L��1 NH4HSO4��Һ�� c(NH4+)��
(3)��Ϊ 0.1 mol��L��1 �ļ��ֵ������Һ��pH ���¶ȱ仯����������ͼ1��ʾ��
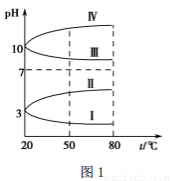
�����з���0.1 mol��L��1 NH4Al(SO4)2��Һ��pH���¶ȱ仯��������________(����������)������ NH4Al(SO4)2��Һ��pH ���¶ȱ仯��ԭ����_____________________��
��20 ��ʱ��0.1 mol��L��1 NH4Al(SO4)2��Һ�� 2c(SO42��)��c(NH4+)��3c(Al3+)��____________ mol��L��1��
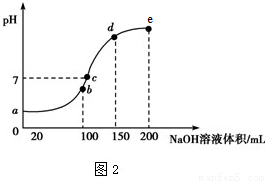
(4)����ʱ����100 mL 0.1 mol��L��1 NH4HSO4��Һ�еμ� 0.1 mol��L��1 NaOH��Һ����ҺpH��NaOH��Һ����Ĺ�ϵ��������ͼ2��ʾ��
�Է���ͼ�� a��b��c��d�ĸ��㣬ˮ�ĵ���̶�������___________�㣬��b�㣬��Һ�и�����Ũ���ɴ�С������˳����_____________________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ĸ�����ѧ��ͳ������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����κ�һ����ѧƽ����ϵ����ȡ���´�ʩ��һ����ʹƽ�ⷢ���ƶ����ǣ� ��
A������һ�ַ�Ӧ�� B��������ϵѹǿ C��ʹ�ô��� D�������¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��CO2(g)+3H2(g) CH3OH(g)+ H2O(g) ��H����49.0 kJ�qmol��1��һ�������£������Ϊ1 L���ܱ������г���1 molCO2��3mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ����
CH3OH(g)+ H2O(g) ��H����49.0 kJ�qmol��1��һ�������£������Ϊ1 L���ܱ������г���1 molCO2��3mol H2�����CO2��CH3OH(g)��Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ����

A��10min�������¶���ʹ ����
����
B��3 minʱ��CO2���������ʵ�����CH3OH�������ʣ��Ҷ���Ũ����ͬ
C�������H2��ƽ��ת����ֻ�ܼ�ѹ��С��Ӧ���������
D���ӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ����v(H2)��0.075 mol�qL-1�qmin-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶��ϰ��ڿ��Ի�ѧ���������棩 ���ͣ������
ԭ���������ε��� �Ҷ�С��36��X��Y��Z��Q��W����Ԫ�أ�����X��ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Qԭ�ӻ�̬ʱ2pԭ�ӹ������2��δ�ɶԵĵ��ӣ�WԪ�ص�ԭ�ӽṹ��3d�ܼ���4��δ�ɶԵ��ӡ��ش��������⣺
�Ҷ�С��36��X��Y��Z��Q��W����Ԫ�أ�����X��ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Qԭ�ӻ�̬ʱ2pԭ�ӹ������2��δ�ɶԵĵ��ӣ�WԪ�ص�ԭ�ӽṹ��3d�ܼ���4��δ�ɶԵ��ӡ��ش��������⣺
��1��Y2X2������Yԭ�ӹ�����ӻ�����Ϊ ��Y2X2�����ЦҼ��ͦм�������Ϊ ��
��2��������ZX3�ķе�Ȼ�����YX4�ĸߣ�����Ҫԭ���� ��
��3��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z������������ķ���ʽ�� ��
��4��Ԫ��W���γɶ��������磺W(CO)5�ȡ�
�ٻ�̬W3+��M������Ų�ʽΪ ��
�� W(CO)5�����³�Һ̬���۵�Ϊ��20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��ж�W(CO)5�������� ����(�������)���þ�����W�Ļ��ϼ�Ϊ ��
W(CO)5�����³�Һ̬���۵�Ϊ��20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��ж�W(CO)5�������� ����(�������)���þ�����W�Ļ��ϼ�Ϊ ��
��5�������йص�˵����ȷ���� ��
A�����Ӿ����У����ۼ�����Խ�÷��Ӿ�����۷е�Խ��
B���縺��˳��X��Y��Z��Q
C����Ϊ������CaO��KCl�ߣ�����KC l��CaO�۵��
l��CaO�۵��
D��H2 YO3�ķ��ӽṹ�к���һ�����ǻ���������Ϊ��ǿ��
��6��Q��Na�γɵ�һ��ֻ�������Ӽ������ӻ�����ľ����ṹ��ͼ4����һ����������Χ���������������Ϊ���㹹�ɵļ�����Ϊ ����֪�þ����ܶ�Ϊ�� g/cm3�������ӵ�����ΪNA�����߳�a= pm��(�ú��ѡ�NA�ļ���ʽ��ʾ)

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶��ϰ��ڿ��Ի�ѧ���������棩 ���ͣ�ѡ����
����FeCl3�������У��ܹ�֤��FeCl3�ǹ��ۻ��������( )
A��FeCl3������ˮ
B��Һ̬��FeCl3������
C��FeCl3�����²��ֽ�
D��FeCl3����ˮ�ܵ��룬������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶���11�¿��Ի�ѧ���������棩 ���ͣ�ѡ����
����˵����ȷ����( )
A��25 ��ʱ���ô�����Һ�ζ���Ũ��NaOH��Һ��pH��7��V ���VNaOH
B������С�մ���Һ�У� c(Na+)��c(HCO3- )
C��Na2CO3��Һ�м�������Ca(OH)2���壬CO32��ˮ��̶ȼ�С����Һ��pH��С
D�������£�����0.10 mol��L��1 �İ�ˮ���� HNO3 ��Һ��ȫ�кͺ���Һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��������и�����ѧ�ڶ�ʱѵ��14��ѧ�Ծ��������棩 ���ͣ�ѡ����
ú̿ȼ���л��������������������Ⱦ������ͼ��ʾ�ĵ����ڽϸ��¶��·�Ӧ�����Ծ����������������жϲ���ȷ���ǣ� ��
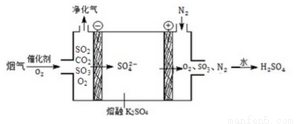
A.��ͼ��֪��������ӦʽΪSO42--2e-��SO2��+O2��
B.SO2��������O2��Ӧ�������������ʽΪSO2+O2+2e-= SO42-
C.����ʧȥ2mol����ʱ�������Ͽ��Եõ���״����11.2L����
D.CO2������缫��Ӧ����������CO2Ũ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ��Ӫ�и��������л�ѧ���������棩 ���ͣ��ƶ���
ijǿ������ҺX�����ܺ���Al3����Ba2����NH4�� ��Fe2����Fe3����CO32-��SO42-��SiO32-��NO3-�е�һ�ֻ������ӣ�ȡ����Һ����ʵ�飬������ת������ͼ����һ�������Ǻ���ɫ����ش��������⣺
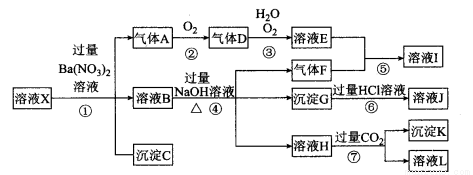
(1)��ҺX�г���H+һ�����ڵ�������________________ ����ҺX��һ�������ڵ�������____________ ��
(2)��������A�����ӷ���ʽΪ________________________________��
(3)ת��������Ӧ������Ϊ__________________________________��
(4)ת�����е����ӷ���ʽΪ___________________________________��
(5)��ת�����У�D��H2O��O2��������ǡ�÷������Ϸ�Ӧ����E����Ӧ��O2��D�����ʵ���֮��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ĸ�����ѧ��ͳ������ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ�������й���Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A��0.1mol/L��������Һ20ml��0.1mol/L����10mL��Ϻ����Һ�У�c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH)
B�����ʵ���Ũ����ȵĢ�NH4C1����(NH4)2SO4����NH4A1(SO4)2������Һ�У�c(NH4+)�ɴ�С��˳��Ϊ����>��>��
C��Ũ��Ϊ0.1mol/L�Ģٰ�ˮ����C6H5ONa��Һ����Na2CO3��Һ����NaHCO3��Һ��pH�Ĵ�С˳��>��>��>��
D��NaHCO3��Һ�У�c(H+)+c(H2CO3)=c(CO32-)+c(OH-)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com