
| A、使石蕊变红的溶液中:Na+、I-、Cl-、NO3-、C6H5O- |
| B、在强碱性溶液中:Na+、K+、[Al(OH)4]-、CO32-、SiO32- |
| C、在无色透明溶液中:NH4+、Fe3+、SO32-、NO3- |
| D、pH=3 的溶液:Na+、Cl-、Fe2+、ClO- |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 关于如图实验的叙述正确的是( )
关于如图实验的叙述正确的是( )| A、X为Cl2.生成Cl2的电极反应:2Cl-→Cl2↑+2e- |
| B、阴极材料必须使用铂做电极 |
| C、在电解过程中,阴极附近的滴液会先呈现红色 |
| D、电解饱和食盐水的化学反应方程式:2NaCl+2H2O=Cl2↑+H2↑+2NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| B、钠与水反应:2Na+2H2O=2Na++2OH-+H2↑ |
| C、氢氧化亚铁溶于稀硝酸中:Fe(OH)2+2H+=Fe2++2H2O |
| D、澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、K+、Na+、
| ||||
B、Ag+、
| ||||
C、Mg2+、H+、
| ||||
D、K+、Na+、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHS溶液水解的方程式为:HS-+H2O?S2-+H3O+ | ||||
| B、向H218O中投入Na2O2固体:2H218O+2Na2O2═4Na++4OH-+18O2↑ | ||||
| C、在100 mL 2 mol/L FeBr2溶液中通入4.48 L氯气(标况下),充分反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | ||||
D、用惰性电极电解饱和氯化钠溶液:2Cl-+2H+
|
查看答案和解析>>
科目:高中化学 来源: 题型:
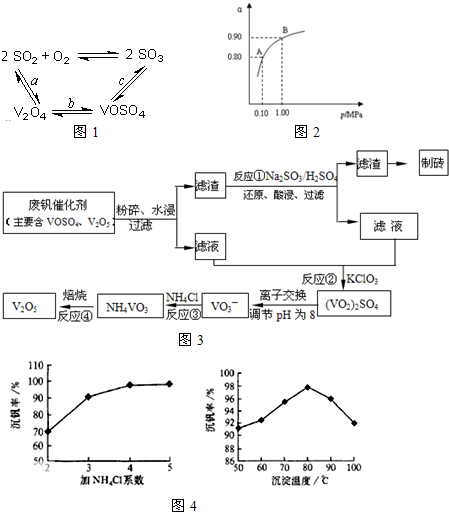
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化硅溶于水显酸性 |
| B、光导纤维传导光的能力非常强,利用光缆通讯,能同时传送大量信息 |
| C、因为高温时二氧化硅与碳酸钠反应放出CO2,所以硅酸的酸性比碳酸强 |
| D、二氧化硅是酸性氧化物,它不溶于任何酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
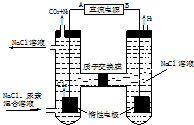 人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如右图.
人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如右图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com