
| ① | ② | ③ | ④ |
| 0.1mol/L NaOH溶液 | pH = 11 NaOH溶液 | 0.1mol/L CH3COOH溶液 | pH = 3 CH3COOH溶液 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
 H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是| A.醋酸溶液中离子浓度的关系满足:c(H+)=c(CH3COO-)+c(OH-) |
| B.物质的量浓度相等CH3COOH和CH3COONa混合溶液: c(CH3COO-)-c(CH3COOH)=2 c(H+)-2 c(OH-) |
C.CH3COOH溶液加水稀释 不变 不变 |
D.CH3COOH溶液加水稀释,溶液中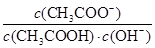 不变 不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH4++ NH2- , 据此判断以下叙述错误的是
NH4++ NH2- , 据此判断以下叙述错误的是 | A.液氨中含有NH3、NH4+、NH2-等粒子 |
| B.一定温度下,液氨中c (NH4+) · c (NH2-) 是一个常数 |
| C.液氨的电离达到平衡时,c (NH3) = c(NH4+) = c (NH2-) |
| D.只要不加入其他物质,液氨中c (NH4+) = c (NH2-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强电解质在溶液中完全电离,不存在电离平衡 |
| B.在溶液里导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
| C.同一弱电解质的溶液,当温度、浓度不同时,其导电能力也不同 |
| D.纯的强电解质在液态时,有的导电,有的不导电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(OH-)/c(NH3·H2O) | B.c(NH3·H2O)/c(OH-) |
| C.n(OH-) | D.c(H﹢) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH4+ + OH– 当其它条件不变时,改变下列条件,平衡向左移动,且c(NH4+)增大的是
NH4+ + OH– 当其它条件不变时,改变下列条件,平衡向左移动,且c(NH4+)增大的是 | A.加NaOH | B.加盐酸 | C.加NH4Cl | D.加热 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
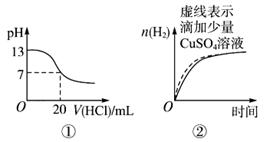
| A.图①表示25 ℃时,用0.1 mol/L盐酸滴定20 mL 0.1mol/L氨水 |
| B.图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应 |
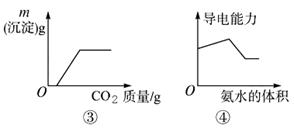
| C.图③表示向CaCl2溶液中通入CO2 |
| D.图④表示向醋酸溶液中滴入氨水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
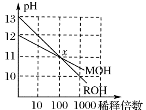
| A.在x点时,ROH完全电离 |
| B.在x点时,c(M+)>c(R+) |
| C.MOH是一种强碱 |
| D.稀释前,c(ROH)=10c(MOH) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H+(溶液)+ In-(黄色溶液)
H+(溶液)+ In-(黄色溶液)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com