
| A. | 铵态氮肥和草木灰?含K2CO3能混合施用 | |
| B. | 化肥和农家肥?如绿肥?不可混合施用 | |
| C. | “盐碱地”中有Na2CO3通过加石膏使之生成碳酸钙,这样根据平衡移动原理,随着c(CO32-)浓度的降低,“盐碱地”的碱性降低 | |
| D. | 复合肥?如磷酸氢二铵?和生石灰能一起施用 |
分析 A.碳酸根离子水解呈碱性,与铵根离子能发生化学反应;
B.化肥和农家肥相互之间无影响;
C.CO32-水解呈碱性,c(CO32-)浓度的降低,碱性减弱;
D.磷酸氢二铵与熟生石灰反应生成氨气.
解答 解:A.碳酸根离子水解呈碱性,与铵态氮肥中的铵根离子能发生化学反应,因此二者不能混合使用,故A错误;
B.化肥和农家肥相互之间无影响,所以化肥和农家肥(如绿肥)可以混合施用,故B错误;
C.“盐碱地”是由CO32-水解呈碱性,c(CO32-)浓度的降低,碱性减弱,故C正确;
D.生石灰与土壤中的水反应生成熟石灰,磷酸氢二铵与熟石灰反应生成氨气,所以复合肥(如磷酸氢二铵)和生石灰一起施用会降低肥效,故D错误;
故选C.
点评 本题考查了化学知识在农业生产中的应用,注意根据常见肥料的性质分析及盐类水解规律的应用,题目比较简单.


科目:高中化学 来源: 题型:解答题
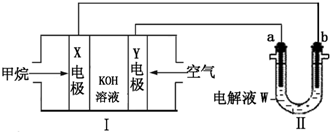
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
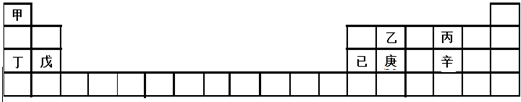
| A. | 乙、丙、辛都是非金属元素 | B. | 甲、丁、戊的单质都是金属 | ||
| C. | 乙、庚、辛都能形成氧化物 | D. | 己的氧化物可与氢氧化钠反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com