
 或
或 或CH2=CHCH2OH.
或CH2=CHCH2OH. 分析 (1)根据商余法来确定有机物的分子式,然后写出结构简式;
(2)若该有机物分子中只有1个氧原子,一个氧原子的式量是16,该有机物的式量是58,剩余的式量是42,则分子式为C3H6O,然后写出结构简式;若该有机物分子中只有2个氧原子,2个氧原子的式量是32,该有机物的式量是58,剩余的式量是26,则分子式为C2H2O2,然后写出结构简式;
(3)据结构中有2个-CH3分析;
(4)若该有机物分子中有-OH,无C=O键,一个羟基的式量是17,该有机物的式量是58,剩余式量是41,则分子式为C3H6O,然后写出结构简式.
解答 解:(1)因某有机物的相对分子质量为58,只由碳、氢两元素组成,根据商余法$\frac{58}{14}$=4…2,所以分子为C4H10,为丁烷,分子组成中含有支链,该有机物的结构简式为(CH3)3CH,
故答案为:(CH3)3CH;
(2)若该有机物分子中只有1个氧原子,一个氧原子的式量是16,该有机物的式量是58,剩余的式量是42,则分子式为C3H6O,分子中有-CH3,则结构简式为:CH3CH2CHO或CH3COCH3,
若该有机物分子中只有2个氧原子,2个氧原子的式量是32,该有机物的式量是58,剩余的式量是26,则分子式为C2H2O2,分子中不会有-CH3,舍去;
故答案为:醛基或羰基;
(3)结构中有2个-CH3,则为CH3COCH3,故答案为:CH3COCH3;
(4)若该有机物分子中有-OH,一个羟基的式量是17,该有机物的式量是58,剩余式量是41,则分子式为C3H6O,无C=O键,则结构简式为: 或
或 或CH2=CHCH2OH,故答案为:
或CH2=CHCH2OH,故答案为: 或
或 或CH2=CHCH2OH.
或CH2=CHCH2OH.
点评 本题主要考查了限制条件下同分异构体的书写,正确推导出分子式的解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖与蔗糖 | |
| B. | O2和O3 | |
| C. | $\left.\begin{array}{l}{12}\\{6}\end{array}\right.$C与$\left.\begin{array}{l}{13}\\{6}\end{array}\right.$C | |
| D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
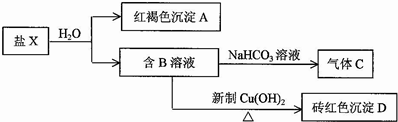
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.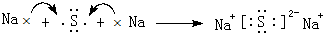 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2COOH | B. | HCOOCH2CH3 | C. | CH3COOCH3 | D. | CH3COCH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | 338 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ②③⑤ | C. | ③④ | D. | ①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com