
 B(OCH3)3 +3H2O�У�H3BO3��ת���ʣ�
B(OCH3)3 +3H2O�У�H3BO3��ת���ʣ�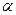 ���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯����ͼ���ɴ�ͼ�ɵó���
���ڲ�ͬ�¶����淴Ӧʱ�䣨t���ı仯����ͼ���ɴ�ͼ�ɵó���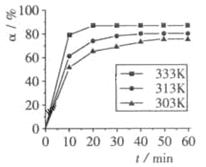
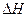 _____0(�<������=����>��).
_____0(�<������=����>��). [B(OH)4]-( aq)+H+��aq��
[B(OH)4]-( aq)+H+��aq�� �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ��ѧʽ | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| ��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ | ��ɫ |
| �ܽ��/g | 1.5��10��4 | 7.1��10��7 | 2.1��10��7 | 1.3��10��16 | 4.3��10��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 _____��B1__________��B2__________��
_____��B1__________��B2__________�� �����ʱ������Һ��ˮ������������ӵ����ʵ���Ũ��֮��Ϊ_______________________ _��
�����ʱ������Һ��ˮ������������ӵ����ʵ���Ũ��֮��Ϊ_______________________ _��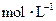 ��
�� ��Һ������Ũ�ȴ�С���� ________________��
��Һ������Ũ�ȴ�С���� ________________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
A���� ���� ���� | B�����Ա�̼��ǿ | C���ѵ� �� �� | D��������ˮ |

 �ı�ֵ �����������С�����䡱����
�ı�ֵ �����������С�����䡱�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3COO�� +H+ ���ڸ�ƽ�⣬����������ȷ���ǣ� ��
CH3COO�� +H+ ���ڸ�ƽ�⣬����������ȷ���ǣ� ��| A����ˮϡ��ʱ����Һ���������ӵ�Ũ����֮��С |
| B����������NaOH���壬ƽ��������Ӧ�����ƶ� |
| C����������0.10 mol��L��1HCl��Һ����Һ��c(H+)���� |
| D����������CH3COONa���壬ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
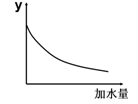
| A����Һ��pH |
| B������ĵ���ƽ�ⳣ�� |
| C����Һ�ĵ������� |
| D������ĵ���̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ˮ�����ᷢ���кͷ�Ӧ |
| B����ˮ��ʹ��ɫʯ��Һ���� |
| C��0.1 mol/L��NH4Cl��Һ��pHֵΪ5.1 |
| D���������ʯ�ҷ�Ӧ�ݳ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| ����(��)����� | ����Ȧ� |
| A.������Һ(��һ����ȫ����)�� HSO  H����SO H����SO | 10% |
B.����������Һ��HSO H����SO H����SO | 29% |
CH3 COOH COOH CH3COO����H�� CH3COO����H�� | 1.33% |
| D.���HCl��H����Cl�� | 100% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com