
����Ŀ����֪��ӦH2(g)+O2(g)=H2O(g)�������仯��ͼ��ʾ��a��b��c��ʾ�����仯��Ϊ��ֵ����λΪkJ������˵����ȷ����
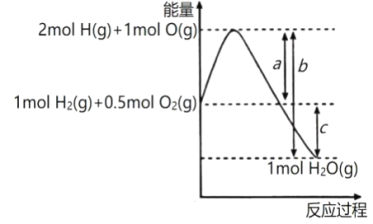
A. �γ�1 mol H2O(g)�еĻ�ѧ����Ҫ����bkJ������
B. 2H2O(g)==2H2(g)+O2(g) ��H=-2(a-b) kJmol-1
C. H2O(l)==H2(g)��O2(g) ��H��ckJ��mol��1
D. 2molH2(g)��1molO2(g)��ȫ��Ӧ����2molH2O(l)�ų�������С��2(b-a) kJ
���𰸡�B
��������A�2molH��g����1molO��g���γ�1molH2O��g���еĻ�ѧ���ͷ�bkJ��������B�����ͼʾH2��g��+1/2O2��g��=H2O��g����H=��a-b��kJ/mol��C����H2O��l����H2O��g������������D�H2O��g����H2O��l���ų�������
A�2molH��g����1molO��g���γ�1molH2O��g���еĻ�ѧ���ͷ�bkJ��������A�����B�����ͼʾH2��g��+1/2O2��g��=H2O��g����H=��a-b��kJ/mol����2H2O��g��=2H2��g��+O2��g����H=-2��a-b��kJ/mol��B����ȷ��C��������ͼʾ��H2O��g��=H2��g��+1/2O2��g����H=ckJ/mol��H2O��l����H2O��g������������H2O��l��=H2��g��+1/2O2��g����H![]() ckJ/mol��C�������D�2molH2��g����1molO2��g����ȫ��Ӧ����2molH2O��g���ų�������Ϊ2��b-a��kJ��H2O��g����H2O��l���ų�������2molH2��g����1molO2��g����ȫ��Ӧ����2molH2O��l���ų�����������2��b-a��kJ��D�����ѡB��
ckJ/mol��C�������D�2molH2��g����1molO2��g����ȫ��Ӧ����2molH2O��g���ų�������Ϊ2��b-a��kJ��H2O��g����H2O��l���ų�������2molH2��g����1molO2��g����ȫ��Ӧ����2molH2O��l���ų�����������2��b-a��kJ��D�����ѡB��


 ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؿ�ѧ�Ҽ��䴴�����۵������У��������( )
A. ��ķ��������Ѹ����ʽģ�� B. �����ٴ�������ѧ˵
C. �Ž��з�����Ԫ�������� D. ¬ɪ������˺�ʽԭ��ģ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����
A. Cl2ͨ��ˮ�У�Cl2 + H2O![]() H+ + Cl��+HClO
H+ + Cl��+HClO
B. CaCO3���������CO![]() + 2H+ = CO2�� + H2O
+ 2H+ = CO2�� + H2O
C. �ö��Ե缫���MgCl2��Һ��2Cl��+2H2O ![]() H2��+ Cl2�� +2OH��
H2��+ Cl2�� +2OH��
D. ����KMnO4��Һ����FeSO4��Һ�У�MnO![]() + Fe2+ + 8H+ = Mn2+ + Fe3+ + 4H2O
+ Fe2+ + 8H+ = Mn2+ + Fe3+ + 4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���γ�����Ĺ�����ͼ��ʾ������˵����ȷ����

A. ��NOx��SO2������������ķ�ɢ����ͬ
B. ���ܳ�������������Ի���������ǿ
C. ������β���е�NOx��Դ��ȼ���еĺ�����
D. �����ữ�������м���ʯ�ҿ��Լ���������γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������豸����ʱ������ѧ��ת��Ϊ���ܵ���
A. ��������� B. ����ӵ�� C. ȼ���� D. ��̫���ܵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��1�¸�����ѧκ����Ŷ���ʯīϩ���ӵ��о�����ȡ����Ҫ��չ�������о���δ����ѧ��������������Ŀ��DZ���������й�̼��������ȷ����
A. ʯī��C60��Ϊͬλ�� B. ���ʯ��̼Ԫ�ص�һ�ֺ���
C. 13C��14C�����ֲ�ͬ��ԭ�� D. 12C��C60Ϊͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Na2CO3��NaHCO3�����ʱȽ��д������( )
A. ��ͬŨ����Һ�ļ���:Na2CO3>NaHCO3B. ��ˮ�е��ܽ��:Na2CO3>NaHCO3
C. ��ͬŨ�ȵ����ᷴӦ�ų����ݵ�����:NaHCO3<Na2CO3D. ���ȶ���:NaHCO3<Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�仯�����������������ʵ�ֵ���
A. Fe��FeCl2B. SO3��H2SO4
C. CO2��COD. KMnO4��MnCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ٽ�״̬�µ�CO2�����ܽ������л��ܼ����ƣ�����ȡ��ҩ�ĵ���Ч�ɷ֣������������¡�����˵��������ǣ� ��
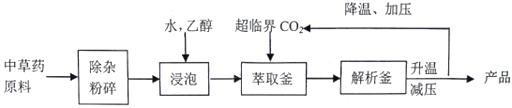
A. ����ʱ�����Ҵ��������в�ҩ��Ч�ɷֵĽ���
B. ���¡���ѹ��Ŀ����ʵ��CO2���Ʒ����
C. ���������¸������ڳ��ٽ�CO2��ȡ
D. CO2������ȡ��ҩ�ľ������ܼ���������ɫ�������ŵ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com