
分析 阴极上阳离子放电顺序为Ag+>Cu2+>H+>Na+,阳极上阴离子放电顺序为Cl->OH->SO42-、NO3-,
(1)当阴极放出H2,阳极放出O2时,则溶液中的电解质不放电,根据离子的放电顺序分析;
(2)当阴极析出金属,则金属离子为Cu2+或Ag+,阳极放出O2时,阴离子为SO42-或NO3-;
(3)当阴极放出H2,则阴极为H+放电,阳极放出Cl2阴离子为Cl-放电;
(4)通过电子的物质的量与阴极析出的金属、阳极析出的气体的物质的量之比为4:2:1时,说明生成1mol气体转移4mol电子,生成1mol金属转移2mol电子.
解答 解:阴极上阳离子放电顺序为Cu2+>H+>Na+,阳极上阴离子放电顺序为Cl->OH->SO42-,
(1)阴极放出H2,阳极放出O2,说明相当于电解水,所以溶质可以是Na2SO4.故答案为:Na2SO4;
(2)在水溶液中Na+不可能放电,所以只能是Cu2+放电.阳极放出O2,说明是OH-放电,所以不能还原氯离子,溶质是CuSO4.故答案为:CuSO4;
(3)阴极放出H2,说明是溶液中的氢离子放电,因此不能含有铜离子.阳极放出Cl2,说明溶液中必须含有氯离子,所以溶质为NaCl.故答案为:NaCl;
(4)阴极析出金属,说明必须含有铜离子.由于阴极析出的铜的物质的量和阳极析出的气体的物质的量之比为2:1,即每生成1mol该气体,反应中就转移4mol电子,所以气体是氧气.故溶质为CuSO4.故答案为:CuSO4.
点评 本题考查电解原理,明确离子的放电顺序是解答本题的关键,注意电极材料与发生的电极反应即可解答,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 光化学烟雾与大量排放碳氢化合物和氮氧化合物有关 | |
| B. | 将草木灰和硫酸铵混合施用,肥效更高 | |
| C. | 棉花的主要成分是纤维素,石英玻璃、陶瓷和水泥均属于硅酸盐产品 | |
| D. | 硫酸工业尾气未经处理就直接排放,将直接导致“温室效应” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a中盛浓盐酸,b中盛浓硫酸 | B. | a中盛浓硫酸,b中盛固体氯化铵 | ||
| C. | f中盛固体氯化钠和浓硫酸 | D. | f中盛固体氯化铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
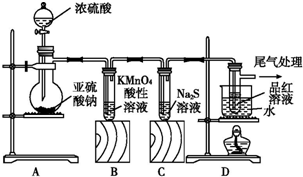
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
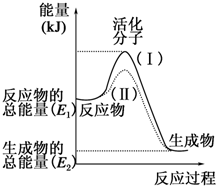 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ•mol-1表示.请认真观察如图,然后回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

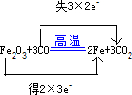 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用装置甲收集SO2并验证其漂白性 | |
| B. | 用装置乙验证氯气与水反应有盐酸生成 | |
| C. | 用澄清石灰水鉴别苏打溶液和小苏打溶液 | |
| D. | 用NaOH溶液除去苯中混有的少量苯酚,反应后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com