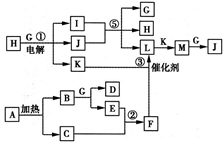
Ў°ҫЖәуЧнјЭЎұіЙОӘЙз»бИИөгОКМвЦ®Т»Ј¬УРТ»ЦЦАлЧУ»ҜәПОпAЈ¬ҝЙУГУЪРЎЖыіө·АЧІұЈ»ӨЖшДТЈ¬јУЗҝ¶ФјЭК»ФұөДұЈ»ӨЈ¬ЖдУЙБҪЦЦФӘЛШЧйіЙЈ¬ДҰ¶ыЦКБҝОӘ65g/molЈ¬јУИИКұҝЙТФЙъіЙБҪЦЦөҘЦКЈ®
GОӘіЈјыИЬјБЈ¬CЎўEЎўKіЈОВПВОӘЖшМ¬өҘЦКЈ¬DКЗТ»ЦЦіЈјыЗҝјоЈ¬·ҙУҰўЪўЫОӘЦШТӘөД№ӨТө·ҙУҰЈ®
Зл»ШҙрПВБРОКМвЈә
ЈЁ1Ј©РҙіцBФЪҝХЖшЦРИјЙХЛщөГІъОпөДөзЧУКҪЈә
Ј®
ЈЁ2Ј©Рҙіц·ҙУҰўЩөДАлЧУ·ҪіМКҪЈә
Ј¬·ҙУҰB+GЎъD+EөДАлЧУ·ҪіМКҪОӘ
2Na+2H2OЁT2Na++2OH-+H2Ўь
2Na+2H2OЁT2Na++2OH-+H2Ўь
Ј®
ЈЁ3Ј©ЧоҪь·ўГчБЛТ»ЦЦәПіЙFөДРВ·Ҫ·ЁЈ¬ФЪіЈС№ПВЈ¬°СEәНC·ЦұрНЁИлТ»ёцјУИИөҪ570ЎжөДөзҪвіШЦРЈ¬ДЬНЁ№эЗвАлЧУөД¶аҝЧМХҙЙ№ММеЧчөзҪвЦКЈ¬EәНCФЪөзј«ЙП·ҙУҰәПіЙБЛFЈ¬ЧӘ»ҜВКҙпөҪ78%Ј¬КФРҙіцөзҪвіШТхј«өДөзј«·ҙУҰКҪЈә
N2+6e-+6H+=2NH3
N2+6e-+6H+=2NH3
Ј®
ЈЁ4Ј©ЖыіөөД°ІИ«ЖшДТДЪУРAөИОпЦКЈ®өұЖыіөФЪёЯЛЩРРК»ЦРКЬөҪГНБТЧІ»чКұЈ¬AОпЦК»бСёЛЩ·ўЙъ·ЦҪв·ҙУҰЈ¬ІъЙъҙуБҝЖшМеЈ¬ідВъЖшДТЈ¬РҙіцAОпЦККЬЧІ»чКұ·ўЙъ·ҙУҰөД»ҜС§·ҪіМКҪЈә
2NaN3=2Na+3N2Ўь
2NaN3=2Na+3N2Ўь
ЈЁОЮРиЧўГч·ҙУҰМхјюЈ©Ј®

 Ў°ҫЖәуЧнјЭЎұіЙОӘЙз»бИИөгОКМвЦ®Т»Ј¬УРТ»ЦЦАлЧУ»ҜәПОпAЈ¬ҝЙУГУЪРЎЖыіө·АЧІұЈ»ӨЖшДТЈ¬јУЗҝ¶ФјЭК»ФұөДұЈ»ӨЈ¬ЖдУЙБҪЦЦФӘЛШЧйіЙЈ¬ДҰ¶ыЦКБҝОӘ65g/molЈ¬јУИИКұҝЙТФЙъіЙБҪЦЦөҘЦКЈ®
Ў°ҫЖәуЧнјЭЎұіЙОӘЙз»бИИөгОКМвЦ®Т»Ј¬УРТ»ЦЦАлЧУ»ҜәПОпAЈ¬ҝЙУГУЪРЎЖыіө·АЧІұЈ»ӨЖшДТЈ¬јУЗҝ¶ФјЭК»ФұөДұЈ»ӨЈ¬ЖдУЙБҪЦЦФӘЛШЧйіЙЈ¬ДҰ¶ыЦКБҝОӘ65g/molЈ¬јУИИКұҝЙТФЙъіЙБҪЦЦөҘЦКЈ®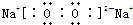
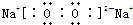
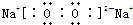 Ј¬№Кҙр°ёОӘЈә
Ј¬№Кҙр°ёОӘЈә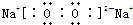 Ј»
Ј»

