
分析 (1)咖啡因分子的相对分子质量=(12×8+1×10+14×4+16×2)=194,根据n=$\frac{m}{M}$计算出0.194g咖啡因的物质的量,然后根据N=nNA计算出含有的咖啡因分子数和N原子数;
(2)根据n=$\frac{m}{M}$、c=$\frac{n}{V}$计算出该泉水中Mg2+的物质的量浓度;根据V=$\frac{n}{c}$计算出含1.0mol Mg2+的这种泉水的体积;
(3)根据V=nVm计算出该硫化氢在标准状况下的体积;分子个数之比等于物质的量之比,结合n=$\frac{m}{M}$计算.
解答 解:(1)0.194g咖啡因的物质的量为:$\frac{0.194g}{194g/mol}$=0.001mol,含有咖啡因分子的数目为:0.001NA,咖啡因的分子式为C8H10N4O2,每个咖啡因分子中含有4个N反应中,则该咖啡因分子中含有N的数目为:0.001NA×4=0.004NA,
故答案为:0.001NA;0.004NA;
(2)4.8×10-2g Mg2+的物质的量为:$\frac{0.048g}{24g/mol}$=0.002mol,该泉水中Mg2+的物质的量浓度为:$\frac{0.002mol}{1.0L}$=0.002mol/L;含1.0mol Mg2+的这种泉水的体积为:$\frac{1.0mol}{0.002mol/L}$=500L,
故答案为:0.002mol/L;500L;
(3)标准状况下0.2molH2S的体积为:22.4L/mol×0.2mol=4.48L;相同质量的CH4和H2S的物质的量与摩尔质量成正比,则其分子个数比=物质的量之比=34g/mol:16g/mol=17:8,
故答案为:4.48;17:8.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积、阿伏伽德罗常数之间的关系即可解答,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:实验题
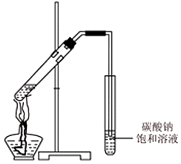 已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.
已知:乙醇是一种非常重要的烃的衍生物,是无色有特殊气味的液体.某化学兴趣小组对乙醇的结构和性质进行了以下探究,请你参与并完成对有关问题的解答.| 实验现象 | 结 论 | |
| ① | 钠沉在乙醇下面 | 钠的密度大于乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl和Na2CO3 | B. | 稀H2SO4和NaHCO3 | C. | CaCl2和Na2CO3 | D. | Ba(OH)2和NaHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
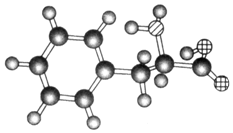
| A. | 该物质的结构简式为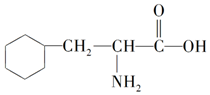 | |
| B. | 该物质可以发生加成反应 | |
| C. | 该物质既可以与强酸反应也可以与强碱反应 | |
| D. | 该物质可以聚合成高分子物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,22.4LCO2含有的分子数为1NA | |
| B. | 常温常压下,1.06gNa2CO3含有的Na+离子数为0.02NA | |
| C. | 通常状况下,NA个CO2分子占有的体积约为22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
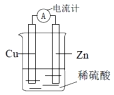
| A. | 该装置中能量转化方式为电能转化为化学能 | |
| B. | 电子从锌片流出,经导线流向铜片 | |
| C. | 工作一段时间之后,溶液颜色逐渐变蓝 | |
| D. | 锌片发生还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com