
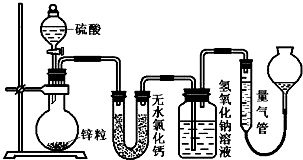
���� ��1������п�������������������������Ӷ�ȷ�������ܵ����˹��
��2�������������Ƶ����ʷ������ص�ԭ��д����Ӧ�Ļ�ѧ��Ӧ����ʽ��
��3������������ԭ��Ӧ���ص������1 molп������������SO2 ���Dz�����������1 molп��Ӧ1 mol���壻
��4��������������ϴ��ƿ���ص��������Ӧ����������ʵ���������������ȥ���ɶ���������Ҫ�����������Ϊ��������������������̶����������������ʵ�����������ˮ�Ȼ��Ƶ����÷�����
��� �⣺��1��Zn+H2SO4=ZnSO4+H2��
1mol 22.4L
$\frac{1.30g}{65g/mol}$=0.02mol 0.448L
0.448L=448mL���������ܵĹ��Ӧ��ѡ500mL��
�ʴ�Ϊ��C��
��2�����������Ǽ�������������壬��������ϴ��ƿ����˵���������������ɣ���п�����ᷴӦʱ��п����ԭ����������������������ԭΪ���������ɣ�1�������֪��1.30gп�����ᷴӦ��ֻ���ɶ�����������0.02mol������Ϊ0.02mol��64g/mol=1.28g���������������ص�����һ�£��ʷ�����Ӧ�Ļ�ѧ����ʽΪ��Zn+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ZnSO4+SO2��+2H2O��
�ʴ�Ϊ��Zn+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ZnSO4+SO2��+2H2O��
��3������������ԭ֪ʶ����ݷ���ʽ��1 molп������������SO2 ���Dz�������������1molп��Ӧ1 mol���壬����������ԭ��Ӧ�е�ʧ��������ȿɵã�$\frac{ag}{65g/mol}$=$\frac{bg}{64g/mol}$+$\frac{��{V}_{2}-{V}_{1}��mL}{22400mL/mol}$��
�ʴ�Ϊ��$\frac{ag}{65g/mol}$=$\frac{bg}{64g/mol}$+$\frac{��{V}_{2}-{V}_{1}��mL}{22400mL/mol}$��
��4��Zn+2H2SO4��Ũ��=ZnSO4+SO2��+2H2O
2mol 1mol
$\frac{m}{32}$mol $\frac{m}{64}$mol
�����ɶ���������Ҫ������Ϊ$\frac{m}{32}$mol��
Zn+H2SO4=ZnSO4+H2��
1mol 1mol
�� cV-$\frac{m}{32}$��mol ��cV-$\frac{m}{32}$��mol
��$\frac{n��{H}_{2}��}{n��S{O}_{2}��}$=$\frac{��cV-\frac{m}{32}��mol}{\frac{m}{64}mol}$=$\frac{64cV-2m}{m}$��
������ʢ����ˮ�Ȼ��Ƶ�U�ܣ���������е�ˮ������������������Һ������ϴ��ƿ�������������Լ���ʱ������������ʵ������������������������ʵ���֮��ƫС��
�ʴ�Ϊ��$\frac{64cV-2m}{m}$��ƫС��
���� ���⿼����Ũ��������ʣ���Ŀ�Ѷ��еȣ���ȷ������Ӧԭ��Ϊ���ؼ���ע�����յ����غ��ڻ�ѧ�����е�Ӧ�ã�������ؿ���ѧ���ķ�����������������ѧʵ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na2SiO3��Һ����μ�������ϡ���SiO32-+2H+�TH2SiO3�����壩 | |
| B�� | ϡFe��NO3��2��Һ�м���ϡ���Fe2++4H++NO3-�TFe3++NO��+2H2O | |
| C�� | ��CuƬ����ϡ�����У�3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O | |
| D�� | ��NH4Al��SO4��2��Һ�м��������Ba��OH��2ϡ��Һ��NH4++Al3++2SO42-+2Ba2++5OH-�T2BaSO4��+NH3•H2O+AlO2-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
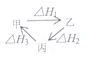
| A�� | �ס��ҡ���������ת����ͼ��ʾ�����H1=��H2+��H3 | |
| B�� | 1molCO��ȫȼ�������ȶ�������ų�����Ϊ283.0KJ����2 CO2��g��=2 CO��g��+O2��g������H=+566.0KJ•mol-1 | |
| C�� | ��N2��g��+3H2��g��?2NH3��g������H=-92.4KJ•mol-1������ij�����г���1mol N2��3molH2��ַ�Ӧ�ų�������Ϊ92.4KJ | |
| D�� | �����£�ϡHCl��ϡNaOH��Һ��Ӧ����1molH2O�ų�����Ϊ57.3 KJ�����Ȼ�ѧ����ʽΪHCl��aq��+NaOH��aq��=NaCl��aq��+H2O��aq������H=-57.3KJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��ɳ�и�����ѧ�ڵ�13���ܲ������ۺϻ�ѧ�Ծ� ���ͣ�ѡ����
����������Ԫ��X��Y��Z��W��ԭ��������������Xԭ�ӵ����������������ڲ��������2����Y�ǵؿ��к�����ߵ�Ԫ�أ�Z2����Y2��������ͬ�ĵ��Ӳ�ṹ��W��Yͬ���塣����˵����ȷ����
A. ZԪ�صļ�������������������Ԫ�صļ����Ӱ뾶��С��
B. Y�ļ���̬�⻯������ȶ��Ա�W��ǿ
C. Y��W�γɵĻ�����һ����ʹ���Ը��������Һ��ɫ
D. ����������Ӧˮ���������X��W��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�������ʡ�������и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��Դ�Ŀ����������������Ŀɳ����Է�չϢϢ��ء�
I����֪��Fe2O3��s����3C��s��=2Fe��s����3CO��g����H1=akJ��mol-1
CO��g����1/2O2��g��=CO2��g����H2=bkJ��mol-1
4Fe��s����3O2��g��=2Fe2O3��s����H3=ckJ��mol-1
��C��ȼ����________kJ��mol-1
��1������ԭ��صĹ���ԭ�������л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص��ǣ�����ţ���
A��C��s��+CO2��g��=2CO��g��
B��NaOH��aq��+HCl��aq��=NaCl��aq��+H2O��1��
C��2H2O��l��=2H2��g��+O2��g��
D��2CO��g��+O2��g��=2CO2��g��
�������ڵ�K2C03��C02Ϊ��Ӧ�Ļ�����������ѡ��Ӧ��Ƴ�һ��ԭ��أ���д����ԭ��صĸ�����Ӧ����
��2��ijʵ��С��ģ�ҵ�ϳɰ���ӦN2��g����3H2��g�� 2NH3��g����H=-92��4kJ��mol-1����ʼ���ǽ�N2��H2�������20mol�������1��1������5L�ϳ����С���ӦǰѹǿΪP������Ӧ������ѹǿ��P��ʾ����Ӧ������P/P����ʱ��t�Ĺ�ϵ����ͼ��ʾ����ش��������⣺
2NH3��g����H=-92��4kJ��mol-1����ʼ���ǽ�N2��H2�������20mol�������1��1������5L�ϳ����С���ӦǰѹǿΪP������Ӧ������ѹǿ��P��ʾ����Ӧ������P/P����ʱ��t�Ĺ�ϵ����ͼ��ʾ����ش��������⣺

�ٷ�Ӧ��ƽ��ı�־�ǣ�����ĸ���ţ���
A��ѹǿ���ֲ���
B�������ܶȱ��ֲ���
C��NH3������������N2���������ʵ�2��
��2minʱ����C��N2���仯��ʾ��ƽ����Ӧ����Ϊ��
�������N2��ת���ʿɲ�ȡ�Ĵ�ʩ�С�
A������ϵ�а������1��1�ٳ���N2��H2
B�������NH3
C�������¶�
D������He��ʹѹǿ����E������һ������N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
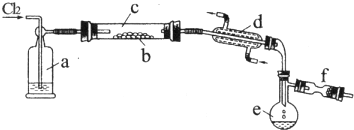
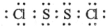 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ݢޢ� | C�� | �٢ڢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ú˴Ź��������Լ����Ҵ��Ͷ����� | |
| B�� |  ��һ�ȴ�����4�� ��һ�ȴ�����4�� | |
| C�� | ����飨 �������к���4�� �������к���4�� | |
| D�� | �����ϩ �� �������������9��ԭ����ͬһƽ���� �������������9��ԭ����ͬһƽ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
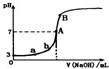
| A�� | ��ͼ��֪HA��һ�����ᣬ��Ka=1.0��10-5 | |
| B�� | ˮ�������������Ũ�ȣ�a��b | |
| C�� | ��NaOH��Һ�����Ϊ10.00mLʱ���У�c��A-��+c��OH-��=c��H+��+c��HA�� | |
| D�� | B����Һ�е�����Ũ�ȹ�ϵΪ��c��Na+����c��A-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com