
| A������NH4����Cl����H����OH�����ӵ���Һ�У�������Ũ��һ���ǣ� c(Cl-)>c(NH4+)> c(H��)> c��OH���� |
| B��pH=6�Ĵ���������ƵĻ����Һ��c(Na+)>c(CH3COO-) |
| C��0.lmol/L��Na2S��Һ�У�c��OH����= c(H��)+ c(HS-)+2 c(H2S) |
| D��pH=3��һ�����pH=11��һ�ּ�������ͺ����Һ��һ����c��OH����=c(H��) |


 ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д� �ƸԴ��ž�ϵ�д�
�ƸԴ��ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��172.5kJ?mol-1 | B��-172.5kJ?mol-1 |
| C��393.5kJ?mol-1 | D��-393.5kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(H��)����l��l0-7mol/L����Һһ����������Һ |
| B�������Ǵ�ˮ���������ԡ����Ի�����ϡ��Һ���ڳ����£���Kw= l��l0-14 |
| C����ˮ���ȣ�Kw����pH���� |
| D���κ�Ũ�ȵ���Һ��������pH����ʾ�����Ե�ǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
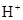 ����c��
����c��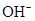 ������ͼ��ʾ��ϵ�������й�˵����ȷ����
������ͼ��ʾ��ϵ�������й�˵����ȷ����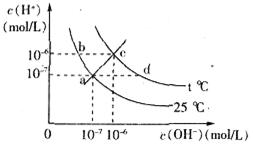
| A��c���Ӧ����Һ�д������ڵ����ӿ���Ϊ��Na����Al3����Cl����CO32�� |
| B����25��ʱ��NaCl��Һ���ȵ�t�棬�����Һ�е�c(OH��)��a��仯��b�� |
| C��t�棾25�� |
| D��ac���ϵ�����һ�����pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Vһ������0.2 |
| B��V���ڻ����0.2 |
C�������Һ������Ũ��һ�����㣺c(Cl��)>c(NH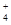 )> c(H��)>c(OH��) )> c(H��)>c(OH��) |
D�������Һ������Ũ��һ�����㣺c(NH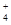 )��c(H��)�� c(Cl��)��c(OH��) )��c(H��)�� c(Cl��)��c(OH��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1molAl3+���Ӻ��еĺ��������Ϊ3NA |
| B��1molCl2������������Ӧ��ת�Ƶĵ�����Ϊ3NA[�� |
| C��10LpH=1��������Һ�к��е�H+������Ϊ2NA |
| D��10LpH=13��NaOH��Һ�к��е�OH-������ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ڸ���Һһ�����ڣ�pH��7 |
| B����c(OH��)>c(H��)������Һ�в����ܴ��ڣ�c(Na��)>c(OH��)>c(A��)>c(H��) |
| C������Һ��c��A-���� c��Na+��������Һһ�������� |
| D��������ΪNaA������Һ��һ�����ڣ�c(Na��)>c(A��)>c(OH-)>c(H��) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com