
【题目】2SO2(g)+O2(g)![]() 2SO3(g),是工业制硫酸的主要反应之一。
2SO3(g),是工业制硫酸的主要反应之一。
(1)该反应过程的能量变化如图所示:

由图中曲线变化可知,该反应为______(填“放热”或“吸热”)反应。该反应通常用V2O5作催化剂,加入V2O5后,改变的是图中的_____。
A.△H B.E C.△H-E D.△H+E
(2)在2L绝热密闭容器中投入2molSO2和bmolO2,下图是部分反应物随时间的变化曲线。

①10min时,v(SO3)=_____。
②反应达到平衡时,SO2的转化率为______。
③下列情况能说明该反应达到化学平衡的是_____
A. v(SO3)=v(SO2) B.混合气体的密度保持不变
C.t时刻,体系的温度不再发生改变 D.混合气体的总物质的量不再改变
【答案】 放热 B 0.05mol/L.min 70% CD
【解析】(1)由图中曲线变化可知反应物总能量高于生成物总能量,因此该反应为放热反应。该反应通常用V2O5作催化剂,加入V2O5后降低活化能,但不能改变反应热,因此改变的是图中的E,答案选B;(2)①由图可知10min时生成三氧化硫是1mol,浓度是0.5mol/L,则v(SO3)=0.5mol/L÷10min=0.05mol/(L·min);②反应达到平衡时生成三氧化硫是1.4mol,则根据方程式可知消耗二氧化硫是1.4mol,SO2的转化率为1.4mol/2mol×100%=70%;③A.v(SO3)=v(SO2)中没有指明反应的方向,则不能说明反应达平衡状态,A错误;B.密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此混合气体的密度保持不变不能说明反应达平衡状态,B错误;C.由于是绝热密闭容器,则t时刻,体系的温度不再发生改变时说明正逆反应速率相等,反应达到了平衡状态,C正确;D.正反应是体积减小的可逆反应,则混合气体的总物质的量不再改变时说明正逆反应速率相等,反应达到了平衡状态,D正确;答案选CD。


科目:高中化学 来源: 题型:
【题目】钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物.
(1)钾和硝酸钾反应可制得K2O(10K+2KNO3→6K2O+N2),39.0g钾与10.1g硝酸钾充分反应生成K2O的质量为g.
(2)某过氧化钾样品中氧的质量分数(杂质不含氧)为0.28,则样品中K2O2的质量分数为 .
(3)超氧化钾和二氧化碳反应生成氧气(4KO2+2CO2→2K2CO3+3O2),在医院、矿井、潜水、高空飞行中用作供氧剂.13.2L(标准状况)CO2和KO2反应后,气体体积变为18.8L (标准状况),计算反应消耗的KO2的质量.
(4)KO2加热至600℃部分分解得到产物A.6.30g产物A充分吸收二氧化碳生成碳酸钾并产生氧气1.12L(标准状况),试确定产物A中钾氧两种原子个数之比.如果产物A只含有两种化合物,写出所有可能的化学式并计算A中两种化合物的物质的量之比.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学式为C3H6Cl2的有机物,若再有一个氢原子被氯原子取代,则产物有两种可能的结构,原有机物的结构简式为( )
A.CH2Cl﹣CH2﹣CH2Cl
B.CHCl2﹣CH2﹣CH3
C.CH2Cl﹣CHCl﹣CH3
D.CH3﹣CCl2﹣CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盛有NO和NO2 的混合气体的量筒倒立在盛有水的水槽中,过一段时间后,量筒内的气体体积减小为原来的一半.
(1)写出有关反应的化学方程式.
(2)原混合气体中NO和NO2的体积比是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关概念间关系的说法正确的是
A. 碱性氧化物一定是金属氧化物
B. 氧化剂在化学反应中一定被氧化
C. 酸性氧化物一定是非金属氧化物
D. 摩尔质量相同的物质其摩尔体积一定相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是周期表前四周期的元素,原子序數依次增大。A的基态原子2p能级上有2个单电子;C是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子,是热和电最佳导体之一;D与F不同周期,但最外能层电子数相等。
(1)写出基态C原子的电子排布式: ____________。
(2)A、B、C三种元素第一电离能最大的是____________。(用元素符号表示),其原因是____________。
(3)B、C两元素形成的化合物B2C的分子空间构型为____________。与B2C互为等电子体的粒子的化学式为____________。(填一种)。
(4)D、E形成的一种离子化合物,在晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为ncm,阿伏加德罗常数为NA,求晶胞的密度ρ=_______g/cm3(用含n、NA的计算式表示)。
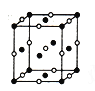
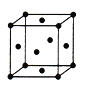
(5)由F原子形成的晶胞结构如图,F原子的半径为r,列式表示F原子在晶胞中的空间利用率:__________________(不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.碳酸氢钠可用于焙制糕点
B.木材纤维和土豆淀粉遇碘水均显蓝色
C.漂白粉可用于游泳池用水的消毒
D.聚乙烯塑料可用于制造包装材料、农用薄膜等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应H2 + Cl2 ![]() 2HCl下列说法中正确的是
2HCl下列说法中正确的是
A. 该反应中,化学能只转变为热能
B. 反应物所具有的总能量高于产物所具有的总能量
C. 产物所具有的总能量高于反应物所具有的总能量
D. 断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成2mol H-Cl键所放出的能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com