
资料:(1)草酸亚铁晶体(FeC2O4·2H2O)呈淡黄色;(2)KMnO4在酸性条件的还原产物为Mn2+。某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究。
(1)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液颜色逐渐变为棕黄色,并检测到CO2生成。这说明草酸亚铁晶体具有 (填“氧化性”、“还原性”或“碱性”)。若反应中消耗1 mol FeC2O4·2H2O,则参加反应的KMnO4为 ______mol。
(2)资料表明:在密闭容器中加热到一定温度时,草酸亚铁晶体可完全分解,生成几种氧化物,残留物为黑色固体。课题组根据课本上所介绍的铁的氧化物的性质,对黑色固体的组成提出如下假设,请你完成假设二和假设三:
假设一:全部是FeO;假设二: ;假设三:
(3)为验证上述假设一是否成立,课题组进行如下研究。
【定性研究】请你完成下表中内容。
| 实验步骤(不要求具体的操作过程) | 预期实验现象和结论 |
| 取少量黑色固体, | |
(共15分)
(1)还原性(1分),0.6(2分)
(2)假设二:全部是四氧化三铁(2分);假设三:氧化亚铁和四氧化三铁的混合物(2分)
(3)[定性研究] 实验步聚:取少量黑色固体,加入适量的稀盐酸(或稀硫酸)溶解(1分),在溶液中加入KSCN溶液(1分)。现象与结论:若溶液不变红,则假设一成立(1分),若溶液变红,则假设一不成立(1分)。
[定量研究]FeC2O4.2H2O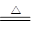 FeO+CO+CO2+2H2O(2分,或FeC2O4
FeO+CO+CO2+2H2O(2分,或FeC2O4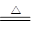 FeO+CO+CO2)
FeO+CO+CO2)
不同意(1分),实验未在密闭容器中进行,FeO会被空气进一步氧化,生成铁的其它氧化物(1分)。
解析试题分析:
(1)结合题中信息可以得出草酸亚铁晶体具有还原性;利用电子守恒1 mol FeC2O4·2H2O中+2价Fe和+3价C分别被氧化为+3价和+4价,所以1 mol FeC2O4·2H2O共失去3mole-,KMnO4在酸性条件的还原产物为Mn2+,1mol KMnO4得到5mol e-,则参加反应的KMnO4为0.6mol。
(2)黑色的铁的氧化物有氧化亚铁和四氧化三铁两种; 根据Fe2+不能使KSCN溶液变红, Fe3+能使KSCN溶液变红,得出定性研究实验步聚、现象与结论。
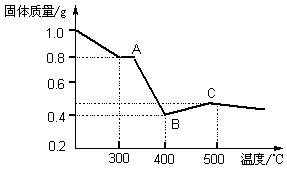
(3)定量研究中,m(FeC2O4·2H2O)="1g," 则n(FeC2O4·2H2O)=1/180mol,FeC2O4·2H2O中H2O的质量分数为1/5,结合图像加热到200℃时间内,是失去水的过程;200℃-400℃时,若C全部转化为CO2,则△m=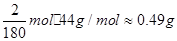 ;若C全部转化为CO,△m=
;若C全部转化为CO,△m=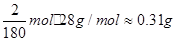 ,实际△m=0.4g,设n(CO2)=xmol,n(CO)="2/180" – xmol。解得x=1/180,所以产物为n(CO2)/ n(CO)=1/1的混合气体可得:FeC2O4.2H2O
,实际△m=0.4g,设n(CO2)=xmol,n(CO)="2/180" – xmol。解得x=1/180,所以产物为n(CO2)/ n(CO)=1/1的混合气体可得:FeC2O4.2H2O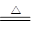 FeO+CO+CO2+2H2O或FeC2O4
FeO+CO+CO2+2H2O或FeC2O4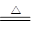 FeO+CO+CO2;实验未在密闭容器中进行,FeO会被空气进一步氧化,生成铁的其它氧化物,而使残留物质量变化。
FeO+CO+CO2;实验未在密闭容器中进行,FeO会被空气进一步氧化,生成铁的其它氧化物,而使残留物质量变化。
考点:本题以探究实验为基础,考查了元素及化合物性质、探究基本方法,氧化还原反应计算,结合图像的化学计算。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:计算题
将5.0g碳酸钙放入一定量稀盐酸中恰好完全反应,得到40mL密度为1.32g/mL的溶液。试计算:
(1)生成标准状况下的二氧化碳气体多少升?(不考虑CO2在水中的溶解)
(2)所得溶液中氯化钙的物质的量浓度。
(3)所用稀盐酸的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学实验小组制备硫酸亚铁铵晶体并设计实验测定其组成,他们进行了以下实验。
Ⅰ.向FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到一种浅蓝绿色的硫酸亚铁铵晶体,这种晶体俗名“摩尔盐”,它比绿矾稳定得多。将摩尔盐低温烘干后,称取7.84 g加热至100 ℃失去结晶水,质量变为5.68 g。
Ⅱ.选择图所示的部分装置连接起来,检查气密性后,将上述5.68 g固体放入A装置的锥形瓶中,再向锥形瓶中加入足量NaOH浓溶液,充分吸收产生的气体并测出气体质量为0.68 g。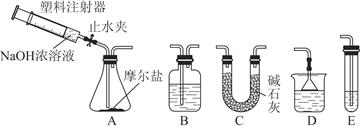
Ⅲ.向A中加入适量3%的H2O2溶液,充分振荡后滤出沉淀,洗净、干燥、灼烧后,测得其质量为1.6 g。
根据上述实验回答下列问题:
(1)实验Ⅰ中,“一系列操作”依次为________、________和过滤,要检验FeSO4溶液中是否含有Fe3+常用的试剂是________。
(2)实验Ⅱ中,选择的装置是A接________接________(填代号),A装置中未使用分液漏斗的理由是____________________________________________________________
(3)向锥形瓶中加入NaOH溶液的操作方法是_________________________________________________________
吸收A中产生的气体所用试剂应是________;实验小组的同学为保证A中产生的气体被完全吸收,以准确测量其质量,他们在A中反应停止后再进行的操作是__________________________________________________________
(4)根据上述实验数据计算,此摩尔盐中,n(NH4+)∶n(Fe2+)∶n(SO42—)∶n(H2O)=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某一种胃药中的抑酸剂为碳酸钙,其中所含的抑酸剂质量的测定如下:
①需配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液
②取一粒(药片质量相同) 0.2 g的此胃药片,磨碎后加入20.0 mL蒸馏水
③以酚酞为指示剂,用0.1 mol·L-1的NaOH溶液滴定,用去V mL达滴定终点
④加入25 mL 0.1 mol·L-1的HCl溶液
(1)写出实验过程的步骤(写编号顺序) 。
(2)下图所示容器中配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号) ,配制上述溶液还需要的玻璃仪器是 (填仪器名称)。 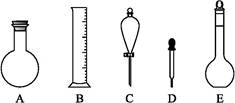
(3)配制上述溶液应选用的容量瓶规格是(填字母) 。
| A.50 mL 50 mL |
| B.100 mL 100 mL |
| C.100 mL 150 mL |
| D.250 mL 250 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
用氯化钠固体配制1.00mol/L的NaCl溶液95mL,回答下列问题
⑴所需仪器为:托盘天平、量筒、烧杯胶头滴管,若要完成实验,还需要两种玻璃仪器为 、 。
⑵该实验的实验步骤为:
①计算,②称量 gNaCl, ③溶解,④移液,⑤洗涤,⑥定容,⑦ 摇匀。
⑶试分析下列操作,对所配溶液的浓度有何影响。(用偏低、偏高、无影响填空)。
①用天平称量氯化钠后,发现砝码底部有锈斑。所配溶液的浓度 ;
②为加速固体溶解,微热烧杯溶液并不断搅拌。在未降至20℃时,就将溶液转移至容量瓶定容。所配溶液的浓度 ;
③容量瓶不干燥,含有少量蒸馏水。所配溶液的浓度 ;
④若定容时仰视刻度线。所配溶液的浓度 ;
⑤定容后,加盖、倒转、摇匀后,发现液面低于刻度线,又补加蒸馏水至刻度。则所配溶液的浓度 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验可行或叙述正确的是 ( )
①.不能用闻气味的方法区分丝织品和棉织物
②.蔗糖加稀硫酸的水解液,再加新制Cu(OH)2悬浊液共热会产生砖红色沉淀
③.乙酸乙酯、油脂在碱性条件下水解均可制肥皂
④.用浓硫酸与蛋白质的颜色反应鉴别部分蛋白质
⑤.金属的冶炼都是置换反应
⑥.漂白粉、玻璃、脂肪是混合物,水银、明矾、蔗糖是纯净物
⑦.盐酸、BaSO4是强电解质,氨水是弱电解质,苯、四氯化碳是非电解质
⑧.符合n(C) :n(H)=n:(2n+2)的物质一定是烷烃
⑨. 煤中含苯及甲苯,可以用先干馏后分馏的方法把它们分离出来
⑩. 离子键只存在于离子化合物中,共价键只存在于共价化合物和离子化合物中
A.⑤⑥⑧⑨⑩ B.①⑥ C.①⑤⑥⑨⑩ D.②③⑦⑨
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于物质分类的说法正确的是
| A.氯化铵、次氯酸都属于强电解质 | B.漂白粉、石英都属于纯净物 |
| C.金刚石、白磷都属于单质 | D.葡萄糖、蛋白质都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质之间的相互关系错误的是( )
| A.CH3CH2OH和CH3OCH3互为同分异构体 |
| B.干冰和冰为同一种物质 |
| C.CH3CH3和CH3CH2CH3互为同系物 |
| D.O2和O3互为同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com