
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
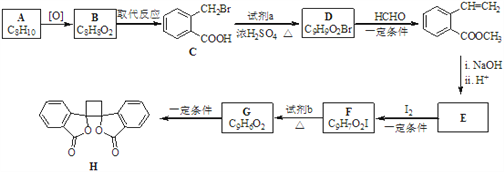
已知:i.RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
ii.R﹣HC═CH﹣R′![]()
![]()
iii.R﹣HC═CH﹣R′![]()
(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是_______________________。
(2)D的结构简式是_______________________________。
(3)由F生成G的反应类型是________________________________________。
(4)由E与I2在一定条件下反应生成F的化学方程式是_____________________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_______________________________。
(5)下列说法正确的是___________(选填字母序号)。
A. G存在顺反异构体
B. 由G生成H的反应是加成反应
C. 1 mol G最多可以与1 mol H2发生加成反应
D. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
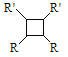
(6)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成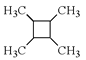 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
【答案】1,2-二甲苯(邻二甲苯)  消去反应
消去反应 
 BD
BD 

【解析】
根据C的结构简式,逆推B是邻甲基苯甲酸;A是邻二甲苯;C在浓硫酸作用下与试剂a反应生成D,根据D的分子式,可推出试剂a是甲醇,D是![]() ;
;![]() 在氢氧化钠作用下发生水解反应,再酸化生成邻乙烯基苯甲酸E;根据信息ii,邻乙烯基苯甲酸E生成F,则F是
在氢氧化钠作用下发生水解反应,再酸化生成邻乙烯基苯甲酸E;根据信息ii,邻乙烯基苯甲酸E生成F,则F是 ,结合信息iii,根据H的结构简式
,结合信息iii,根据H的结构简式 ,逆推G是
,逆推G是![]() 。
。
(1)芳香烃是指含有苯环的碳氢化合物。A的化学式为C8H10,根据碳原子个数可知A中含有一个苯环,剩余含有2个碳原子的取代基取代苯环上的氢原子,苯环上的取代基可能为1个乙基或2个甲基。根据物质C中苯环上的取代基位置关系可知,A的结构简式为 ,则A的名称为1,2-二甲苯(或邻二甲苯)。
,则A的名称为1,2-二甲苯(或邻二甲苯)。
因此,本题正确答案是:1,2-二甲苯(邻二甲苯);
(2)由“已知ⅰ”可知:物质D与甲醛反应,脱去一个溴原子和一个氢原子,并与甲醛中的碳原子形成碳碳双键,则物质D的结构式为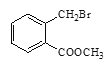 。
。
因此,本题正确答案是: ;
;
(3)根据以上分析,F是 ,G是
,G是![]() ,F中碘原子与邻位碳原子上的氢原子发生消去反应形成碳碳双键。
,F中碘原子与邻位碳原子上的氢原子发生消去反应形成碳碳双键。
因此,本题正确答案是:消去反应;
(4)E的结构简式为 ,根据“已知ⅱ”,E的结构简式中有碳碳双键和羧基,在一定条件下与I2反应时,断去碳碳双键,同时两个碳原子分别连接一个碘原子和一个酯基,生成物质F。因此,物质E生成物质F的方程式为:
,根据“已知ⅱ”,E的结构简式中有碳碳双键和羧基,在一定条件下与I2反应时,断去碳碳双键,同时两个碳原子分别连接一个碘原子和一个酯基,生成物质F。因此,物质E生成物质F的方程式为: 。
。
邻乙烯基苯甲酸与I2在一定条件下反应生成F的产物不唯一,此反应同时生成另外一种有机副产物且与F互为同分异构体,此有机副产物的结构简式是 。
。
因此,本题正确答案是: ;
; ;
;
(5)A项,顺反异构体形成的条件包括:①存在限制旋转的因素,如双键;②每个不能旋转的碳原子都连接两个不同的原子或原子团。G中形成双键的一个碳原子连接2个氢原子,不符合条件②,因此不存在顺反异构体,故A项错误;
B项,由G生成H的过程中,碳碳双键打开,结合成四个碳碳单键,属于加成反应,故B项正确;
C项,物质G中可与氢气发生加成的官能团有苯环和碳碳双键,因此物质G最多能与4 mol H2发生加成反应,故C项错误。
D项,F的结构简式为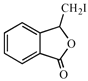 ,其中酯基和碘原子均可与NaOH发生反应,则1 mol 的F最多可与2 molNaOH反应;而H的结构简式中含有两个酯基,与NaOH发生水解反应,因此1mol的H最多可消耗2 molNaOH,故D项正确。
,其中酯基和碘原子均可与NaOH发生反应,则1 mol 的F最多可与2 molNaOH反应;而H的结构简式中含有两个酯基,与NaOH发生水解反应,因此1mol的H最多可消耗2 molNaOH,故D项正确。
因此,本题正确答案是:BD。
(6)本题采用逆推法。由“已知ⅲ”可知,要合成物质 的反应物为CH3CH=CHCH3。要在乙烯的基础上增长碳链的同时形成碳碳双键,可运用“已知ⅰ”,即用溴乙烷与乙醛作为反应物,生成CH3CH=CHCH3,因此只需将乙烯作为反应物,溴乙烷可以通过乙烯加成反应得到,乙醛可以通过乙烯先加成后氧化得到。
的反应物为CH3CH=CHCH3。要在乙烯的基础上增长碳链的同时形成碳碳双键,可运用“已知ⅰ”,即用溴乙烷与乙醛作为反应物,生成CH3CH=CHCH3,因此只需将乙烯作为反应物,溴乙烷可以通过乙烯加成反应得到,乙醛可以通过乙烯先加成后氧化得到。
合成路线如图所示:

 。
。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列有关四个常用的电化学装置的叙述,正确的是( )
A.图 所示碱性锌锰电池中,MnO2是催化剂
所示碱性锌锰电池中,MnO2是催化剂
B.图 所示铅蓄电池放电过程中,硫酸浓度保持不变
所示铅蓄电池放电过程中,硫酸浓度保持不变
C.图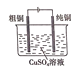 所示电解精炼铜装置工作过程中,电解质溶液中Cu2+浓度不断增大
所示电解精炼铜装置工作过程中,电解质溶液中Cu2+浓度不断增大
D.图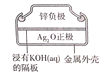 所示纽扣式锌银电池工作过程中,外电路中电子由锌极流向氧化银极
所示纽扣式锌银电池工作过程中,外电路中电子由锌极流向氧化银极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜是一种重要的化工产品,常用作有机合成催化剂,还可用于颜料,防腐等工业。查阅资料得知:CuCl是一种白色固体,微溶于水,不溶于酒精,能溶于浓盐酸,其熔融物导电性很差。
(1)CuCl为__________(填“共价化合物”或“离子化合物”)。
(2)在CuCl2溶液中逐滴加入过量 KI溶液可能发生:
a.2Cu2++4I-=2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-=2CuCl↓(白色)+I2
若a反应为主要反应,则Ksp(CuI)________Ksp(CuCl)(填“>”、“<”或“=”=)
(3)实验室可用氯化铜溶液、铜粉、浓盐酸反应制备氯化亚铜,其反应原理和流程为:
CuCl2+Cu+2HCl(浓)![]() 2HCuCl2(无色)
2HCuCl2(无色)![]() 2CuCl↓(白色)+2HCl
2CuCl↓(白色)+2HCl

①上述反应流程中,加入氯化钠的目的是________________________。
②常温下,CuOH的Ksp为1.0×10-14,则Cu++H2O![]() CuOH+H+的平衡常数为:________
CuOH+H+的平衡常数为:________
③为得到纯净的CuCl晶体,最好选用__________(填编号)试剂进行洗涤。
a.蒸馏水 b.稀硫酸 c.氯化铜溶液 d.乙醇
④CuCl在潮湿的环境中易被氧化为Cu2(OH)3Cl,反应的化学方程式为__________。实验时,若用2mL0.5mol/L的CuCl2 溶液,最终可得到产品0.16g,则实验的产率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在第n电子层中,当它作为原子的最外电子层时,最多容纳的电子数与n-1层相同,当它作为原子的次外层时,其电子数比n+1层最多能多10个,则此电子层是( )
A.K层B.M层
C.L层D.N层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:H2(g)+![]() O2(g)=H2O(g) △H1
O2(g)=H2O(g) △H1
![]() N2(g)+O2(g)=NO2(g) △H2
N2(g)+O2(g)=NO2(g) △H2
![]() N2(g)+
N2(g)+![]() H2(g)=NH3(g) △H3
H2(g)=NH3(g) △H3
则反应2NH3(g)+![]() O2(g)=2NO2(g)+3H2O(g)的△H为
O2(g)=2NO2(g)+3H2O(g)的△H为
A. 2△H1+2△H2-2△H3 B. △H1+△H2-△H3
C. 3△H1+2△H2+2△H3 D. 3△H1+2△H2-2△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,可逆反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0。达到平衡,当单独改变下列条件后,有关叙述错误的是
2NH3(g) ΔH<0。达到平衡,当单独改变下列条件后,有关叙述错误的是
A. 加催化剂v正、v逆都发生变化,而且变化的倍数相等
B. 加压v正、v逆都增大,且v正增大的倍数大于v逆增大的倍数
C. 降温,v正、v逆都减小,且v正减小的倍数小于v逆减小的倍数
D. 加入氩气,v正、v逆都增大且v正增大的倍数大于v逆增大的倍数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应2A(g)+B(g) ![]() 2C(g),根据下表中的数据判断下列图像错误的是
2C(g),根据下表中的数据判断下列图像错误的是
压强 A的转化率 温度 | P1(MPa) | P2(MPa) |
400℃ | 99.6% | 99.7% |
500℃ | 96.9% | 97.8% |
A.  B.
B. 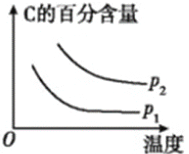 C.
C.  D.
D. 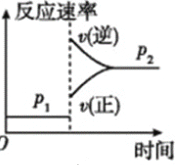
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式与事实相符且书写正确的是( )
A. 炼铁高炉中生成铁:3C+2Fe2O3![]() 4Fe+3CO2↑
4Fe+3CO2↑
B. 铝放入稀硫酸中:Al+H2SO4=AlSO4+H2↑
C. 向氢氧化钠溶液中加入硫酸铜溶液:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
D. 向小苏打中滴加稀硫酸: Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 向0.1 mol·L1 Na2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. 常温下,pH=6的NaHSO3溶液中:c(![]() )c(H2SO3)=9.9×107 mol·L1
)c(H2SO3)=9.9×107 mol·L1
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:![]() <
<![]()
D. 0.1 mol·L1 Na2C2O4溶液与0.1 mol·L1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com