
填写下列空白(7分):
(1)写出表示含有8个质子、10个中子的原子的化学符号:___________。
(2)周期表中位于第8纵行的铁元素属于第 族。
(3)周期表中最活泼的非金属元素位于第 纵行。
(4)所含元素超过18种的周期是第 、 周期
(5)请写出298K,101KPa时,下列反应的热化学方程式:
用CO(g)还原1mol Fe2O3(s)放热24.8KJ 。
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源:2014-2015学年天津市和平区高三下学期第一次质量调查化学试卷(解析版) 题型:实验题
(18分)Ⅰ.实验室制备一氧化碳原理是:HCOOH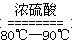 H2O+CO↑。
H2O+CO↑。
(1)从下图挑选所需的仪器,画出Ⅰ中所缺的气体发生装置,并标明容器中的试剂。
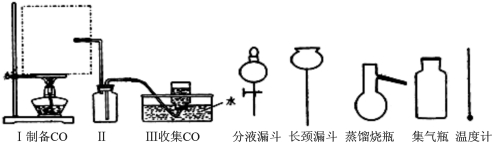
(2)装置Ⅱ的作用是 。
Ⅱ.实验室制备四水甲酸铜[Cu(HCOO)2·4H2O]晶体实验步骤如下:
(1)碱式碳酸铜的制备:
a、步骤ⅰ是将一定量胆矾和NaHCO3固体一起放到研钵中研磨,其目的是 。
b、步骤ⅱ是在搅拌下将固体混合物分多次缓慢加入热水中,反应温度控制在70℃—80℃,如果看到 (填写实验现象),说明温度过高。
c、相关的化学方程式是 。
(2)四水甲酸铜[Cu(HCOO)2·4H2O]晶体的制备:
将碱式碳酸铜固体放入烧杯中,加入一定量热的蒸馏水,再逐滴加入甲酸至碱式碳酸铜恰好全部溶解,趁热过滤除去少量不溶性杂质。然后蒸发,冷却,过滤,再用少量无水乙醇洗涤晶体2—3次,晾干,得到产品。
a、相关的化学方程式是 。
b、“趁热过滤”中,必须“趁热”的原因是 。
c、用乙醇洗涤晶体的目的是 。
Ⅲ.探究小组用滴定法测定四水甲酸铜[Cu(HCOO)2·4H2O](Mr=226)含量。取a g试样配成100 mL溶液,每次取20.00 mL,消除干扰离子后,用c mol /L-1 EDTA(H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液6 mL。滴定反应如下:Cu2++H2Y2- =CuY2-+2H+,写出:(1)计算Cu(HCOO)2·4H2O质量分数的表达式ω=______;
(2)下列操作会导致Cu(HCOO)2·4H2O含量的测定结果偏高的是___________。
a.未干燥锥形瓶
b.滴定终点时滴定管尖嘴中产生气泡
c.未除净可与EDTA反应的干扰离子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省绥化市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
[化学---选修3:物质结构与性质] (15分)太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)铟与镓同是IIIA族元素,写出铟基态原子的电子排布式: 。
(2)硒为第四周期VIA族元素,与其相邻的元素有砷(33号)、溴(35号),则三种元素的电负性由小到大的顺序为 。(用元素符号表示)
(3)SeO3分子的立体构型为 。
(4)硅烷(SinH2n+2)的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是 。
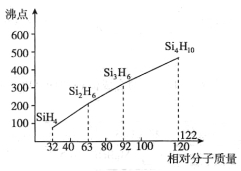
(5)硼元素具有缺电子性,其化合物往往具有加合性,如硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-,其中B原子的杂化类型为 。
(6)金属铜投入氨水中或投入H2O2溶液中均无明显现象,但投入氨水—过氧化氢混合液中,则铜片溶解,溶液呈深蓝色,写出该反应的离子方程式: 。
(7)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数比为 ;若该晶体的晶胞参数为a pm,则该合金密度为 g/cm3。(列出计算式,不要求计算结果,阿伏伽德罗数的值为NA)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三第二次联考理综化学试卷(解析版) 题型:实验题
(15分)以下是某学习小组对乙二酸的某些性质进行研究性学习的过程:
[研究课题]探究乙二酸的某些性质
[查阅资料]乙二酸(HOOC-COOH)俗称草酸,草酸晶体的化学式为H2C2O4·2H2O;草酸在100℃时开始升华,157℃时大量升华,并开始分解;草酸蒸气在低温下可冷凝为固体;草酸钙不溶于水,草酸蒸气能使澄清石灰水变浑浊。
[提出猜想]
猜想一:乙二酸具有不稳定性
根据草酸晶体的组成,该小组同学猜想其受热分解产物为CO、CO2和H2O。
设计方案:
(1)请用下列装置组成一套探究并验证其产物的实验装置(草酸晶体分解装置略,连接导管略去)。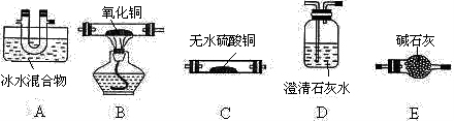
请回答下列问题:
①装置的连接顺序为:A→( )→D→( )→B→D。
②装置中碱石灰的作用是 。实验时,在点燃B处酒精灯之前,应进行的操作是 。检验产物中CO的实验现象是 。③整套装置存在不合理之处为 。
猜想二:乙二酸具有弱酸性
设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是______(填字母)。
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(3)该小组同学将2.52 g草酸晶体M(H2C2O4·2H2O)=126g/mol加入到100 mL 0.2 mol/L的NaOH溶液中充分反应,使用pH计测定反应后溶液,结果呈酸性,则溶液中各离子的浓度由大到小的顺序为 。
猜想三:乙二酸具有还原性设计方案:
(4)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性。该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省六校高三第二次联考理综化学试卷(解析版) 题型:选择题
下列有关实验原理或操作正确的是
A.实验室将硫酸铜溶液直接加热蒸发至干方法来制取CuSO4·5H2O
B.用KSCN溶液检验硫酸亚铁溶液是否氧化变质
C.用湿润的pH试纸来检验溶液的pH值
D.用四氯化碳萃取溴的苯溶液中的溴
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一下学期第一次月考化学试卷(解析版) 题型:选择题
短周期元素W、X、Y和Z的原子序数依次增大。元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
A.元素W、X的氯化物中,各原子均满足8电子的稳定结构
B.元素X与氢形成的原子比为1:1的化合物有很多种
C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成
D.元素Z可与元素X形成共价化合物XZ2
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于C、Si、S、Cl四种非金属元素的说法中,正确的是
A.在自然界中都能以游离态存在
B.两两结合形成的化合物都是共价化合物
C.氢化物的热稳定性比较:CH4 < SiH4 < H2S < HCl
D.最高价氧化物都能与水反应生成相应的酸,且酸性依次增强
查看答案和解析>>
科目:高中化学 来源:2014-2015上海市奉贤区高三第二学期调研测试化学试卷(解析版) 题型:选择题
向次氯酸钙溶液中通入一定量SO2,可能出现的离子方程式为
A.Ca2+ + ClO— + SO2 + H2O → CaSO4↓ + Cl— + 2H+
B.Ca2+ + 2ClO— + 2SO2 + 2H2O → CaSO4↓ + 2Cl— + 2H+ + SO42—
C.Ca2+ + 3ClO— + 3SO2 + 3H2O → CaSO4↓ + 3Cl— + 6H+ + 2SO42—
D.Ca2+ + 3ClO— + SO2 + H2O → CaSO4↓ + 2HClO + Cl—
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省肥城市高三二模理综化学试卷(解析版) 题型:选择题
几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是
元素代号 | X | Y | Z | M | R | Q | |
原子半径(×10—10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | —— |
最低负价 | —— | —1 | —— | —— | —3 | —2 | |
A.X、Z、R的最高价氧化物的水化物之间可两两相互反应
B.元素X和Q形成的化合物中不可能含有共价键
C.X、Z、M的单质分别与水反应,M最剧烈
D.Y的氢化物的水溶液可用于雕刻玻璃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com