
【题目】在100g浓度为ω%的稀硫酸中加入4g氧化铜粉末,待氧化铜全部溶解后,向所得蓝色溶液中加入10g铁粉,充分反应后,过滤,得滤液和4.8g滤渣.下列计算结果正确的是
A.4.8g滤渣是由3.2g铜和1.6g铁组成B.ω=14.7
C.反应过程中产生的氢气是2.24LD.滤液是20.88%的硫酸亚铁溶液
【答案】AB
【解析】
所得滤渣中铜元素的质量与氧化铜中铜元素的质量相等,则铜的质量为:4g![]() =32g,故滤渣中铁的质量为4.8g-3.2g=1.6g,设生成3.2g铜需要铁的质量为x,
=32g,故滤渣中铁的质量为4.8g-3.2g=1.6g,设生成3.2g铜需要铁的质量为x,
Fe+CuSO4=FeSO4+Cu
56 64
x 3.2g
![]() ,解得x=2.8g,而剩余的滤渣中含铁的质量是1.6g,故与硫酸反应的铁的质量为:10g-2.8g-1.6g=5.6g,设生成的氢气的质量为z,
,解得x=2.8g,而剩余的滤渣中含铁的质量是1.6g,故与硫酸反应的铁的质量为:10g-2.8g-1.6g=5.6g,设生成的氢气的质量为z,
Fe+H2SO4=FeSO4+H2↑
56 2
5.6g z
![]() =
=![]() ,解得z=0.2g,反应中硫酸全部转化生成硫酸亚铁,根据铁、硫酸和硫酸亚铁的质量关系,设消耗的硫酸的质量为a,生成的硫酸亚铁的质量为b
,解得z=0.2g,反应中硫酸全部转化生成硫酸亚铁,根据铁、硫酸和硫酸亚铁的质量关系,设消耗的硫酸的质量为a,生成的硫酸亚铁的质量为b
Fe~ H2SO4~ FeSO4
56 98 152
8.4g a b
![]() =
=![]() =
=![]() ,解得a=14.7 b=22.8g 。
,解得a=14.7 b=22.8g 。
A、根据计算可知4.8g的滤渣是由3.2g铜和1.6g铁组成,故A正确;
B、硫酸溶液的质量分数为:![]() 1=14.7
1=14.7![]() ,故B正确;
,故B正确;
C、状况不知,无法求气体体积,故C错误;
D.硫酸亚铁溶液的质量分数为:![]() /
/![]() =20.9
=20.9![]() ,故D错误;
,故D错误;
答案为AB。


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
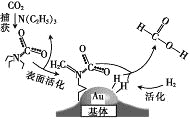
A. 标准状况下,22.4L CO2中所含的电子数目为16NA
B. 10.1g N(C2H5)3中所含的非极性共价键数目为0.3NA
C. 2mol Au与2mol H2中所含的分子数目均为2NA
D. 100g 46%的甲酸水溶液中所含的氧原子数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验可达到实验目的的是
A.用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液
B.向CH3CH2Br中滴入AgNO3溶液以检验溴元素
C.用溴的四氯化碳溶液吸收SO2气体
D.![]() 与NaOH的醇溶液共热制备CH3-CH=CH2
与NaOH的醇溶液共热制备CH3-CH=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数的值为NA,下列说法正确的是( )
A.1mol苯乙烯中含有的![]() 键数为4NA
键数为4NA
B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.0.1molCnH2n+2中含有的C—C键数为0.1nNA
D.标准状况下,2.24LCCl4中含有的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图1,主要步骤如下:
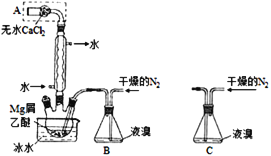
图1 图2
步骤1、三颈瓶中装入10g镁屑和150mL无水乙醚;装置B中加入15mL液溴;
步骤2、缓慢通入干燥的氮气,直至溴完全导入三颈瓶中;
步骤3、反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品;
步骤4、室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MgBr2产品。
已知:①Mg与Br2反应剧烈放热;MgBr2具有强吸水性;
②MgBr2+3C2H5OC2H5![]() MgBr23C2H5OC2H5
MgBr23C2H5OC2H5
请回答:
(1)仪器A的名称是______;
(2)实验中不能用干燥空气代替干燥N2,原因是______________;
(3)步骤3中,第一次过滤除去的物质是_________________;
(4)有关步骤4的说法,正确的是__________________;
A.可用95%的乙醇代替苯溶解粗品 B.洗涤晶体可选用0℃的苯
C.加热至160℃的主要目的是除去苯 D.该步骤的目的是除去乙醚和可能残留的溴
(5)为测定产品的纯度,可用EDTA(简写为Y)标准溶液滴定,反应的离子方程式:Mg2++Y4﹣═MgY2
①滴定管洗涤前的操作是_______________________;
②测定时,先称取0.2500g无水MgBr2产品,溶解后,用0.0500molL﹣1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液25.00mL,则测得无水MgBr2产品的纯度是__________(以质量分数表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,且四种元素的原子最外层电子数之和为24。下列说法错误的是
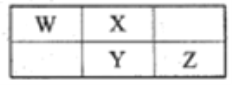
A. 单核阴离子的还原性Y强于X
B. W的气态氢化物与其最高价含氧酸反应生成离子化合物
C. X、Y、Z最简单氢化物中稳定性最弱的是Y
D. 在元素周期表中118号元素与Z位于同一主族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计能够成功的是
A.除去粗盐中含有的硫酸钙杂质
![]()
B.检验亚硫酸钠试样是否变质
![]()
C.证明酸性条件H2O2的氧化性比I2强
![]()
D.检验某溶液中是否含有 Fe2+
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用人工模拟光合作用合成甲酸的原理为2CO2+2H2O=2HCOOH+O2,装置如图所示,下列说法不正确的是( )
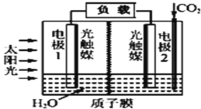
A.该装置能将太阳能转化为化学能和电能
B.电子由电极1经过负载流向电极2
C.电极2的反应式:CO2+2H++2e-=HCOOH
D.电极1周围pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com