
”¾ĢāÄæ”æĻĀĮŠµÄ·ÖĄė·½·Ø²»ÕżČ·µÄŹĒ( )”£
A£®ÓĆ¾Ę¾«ŻĶČ”µāĖ®ÖŠµÄµā
B£®ÓĆÕōĮóµÄ·½·Ø½«×ŌĄ“Ė®ÖĘ³ÉÕōĮóĖ®
C£®ÓĆ¹żĀĖµÄ·½·Ø³żČ„Ź³ŃĪĖ®ÖŠµÄÄąÉ³
D£®ÓĆĢŌĻ“µÄ·½·Ø“ÓɳĄļĢŌ½š

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA“ś±ķ°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠ±ķŹöÕżČ·µÄŹĒ
A£®½«NAøöNH3·Ö×ÓĘųĢåČÜÓŚ1LĖ®ÖŠµĆµ½1mol”¤L£1µÄ°±Ė®
B£®22.4L¶žŃõ»ÆĮņ·Ö×ÓÖŠµē×Ó×ÜŹżŌ¼ĪŖ32NA
C£®1 mol NaÓė×ćĮæO2·“Ӧɜ³ÉNa2O»ņNa2O2¾łŹ§Č„NAøöµē×Ó
D£®ø÷5.6 gĢś·Ö±šÓė×ćĮæµÄŃĪĖį”¢ĀČĘų·“Ó¦£¬µē×Ó×ŖŅĘ×ÜŹż¾łĪŖ0.3NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒāŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļÖÖĄąÖŚ¶ą£¬ŌŚĻĀĮŠ»ÆŗĻĪļÖŠ£¬ĒāŌŖĖŲĻŌŹ¾Õż¼ŪµÄŹĒ
A£®BH3 B£®SiH4 C£®C2H2 D£®NaH
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ1-äå±ūĶéŹĒŅ»ÖÖÖŲŅŖµÄÓŠ»śŗĻ³ÉÖŠ¼äĢ壬·ŠµćĪŖ71”ę£¬ĆܶČĪŖ1.36 g”¤cm-3”£ŹµŃéŹŅÖʱøÉŁĮæ1-äå±ūĶéµÄÖ÷ŅŖ²½ÖčČēĻĀ:
²½Öč1:ŌŚŅĒĘ÷AÖŠ¼ÓČė½Į°č“Å×Ó”¢12 gÕż±ū“¼¼°20 mLĖ®£¬±łĖ®ĄäČ“ĻĀ»ŗĀż¼ÓČė28 mLÅØH2SO4;ĄäČ“ÖĮŹŅĪĀ£¬½Į°čĻĀ¼ÓČė24 g NaBr”£
²½Öč2:ČēĶ¼ĖłŹ¾“ī½ØŹµŃé×°ÖĆ£¬»ŗĀż¼ÓČČ£¬Ö±µ½ĪŽÓĶדĪļĮó³öĪŖÖ¹”£
²½Öč3:½«Įó³öŅŗ×ŖČė·ÖŅŗĀ©¶·£¬·Ö³öÓŠ»śĻą”£
²½Öč4:½«·Ö³öµÄÓŠ»śĻą×ŖČė·ÖŅŗĀ©¶·£¬ŅĄ“ĪÓĆ12 mL H2O”¢12 mL 5% Na2CO3ČÜŅŗŗĶ12 mL H2OĻ“µÓ£¬·ÖŅŗ£¬µĆ“Ö²śĘ·£¬½ųŅ»²½Ģį“æµĆ1-äå±ūĶ锣

£Ø1£©ŅĒĘ÷AµÄĆū³ĘŹĒ_____________;¼ÓČė½Į°č“Å×ÓµÄÄæµÄŹĒ·ĄÖ¹±©·ŠŗĶ___________________”£
£Ø2£©·“Ó¦Ź±Éś³ÉµÄÖ÷ŅŖÓŠ»śø±²śĪļÓŠ2-äå±ūĶéŗĶ__________________________________”£
£Ø3£©²½Öč2ÖŠŠčĻņ½ÓŹÜĘæÄŚ¼ÓČėÉŁĮæ±łĖ®²¢ÖĆÓŚ±łĖ®Ō”ÖŠµÄÄæµÄŹĒ___________________”£
£Ø4£©²½Öč2ÖŠŠč»ŗĀż¼ÓČČŹ¹·“Ó¦ŗĶÕōĮóĘ½ĪČ½ųŠŠ£¬ÄæµÄŹĒ______________________________”£
£Ø5£©²½Öč4ÖŠÓĆ5%Na2CO3ČÜŅŗĻ“µÓÓŠ»śĻąµÄ²Ł×÷: Ļņ·ÖŅŗĀ©¶·ÖŠŠ”ŠÄ¼ÓČė12 mL 5% Na2CO3ČÜŅŗ£¬Õńµ“£¬____________£¬¾²ÖĆ£¬·ÖŅŗ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČŹ±£¬ŌŚŅ»øöČŻ»żĪŖ3LµÄĆܱÕČŻĘ÷ÖŠ£¬A”¢B”¢CČżÖÖĘųĢ¬ĪļÖŹµÄĪļÖŹµÄĮæĖꏱ¼ä±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£Ēė»Ų“šŅŌĻĀĪŹĢā£ŗ
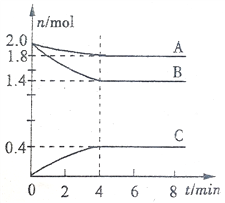
£Ø1£©øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_________________________________”£
£Ø2£©·“Ó¦“ÓæŖŹ¼µ½Ę½ŗāŹ±£¬ĘųĢåBµÄĘ½¾ł·“Ó¦ĖŁĀŹŹĒ___________________”£
£Ø3£©øĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ŹĒ______________________________”£
£Ø4£©ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Äę·“Ó¦ĖŁĀŹ½«____________£ØĢī”°¼Óæģ”±”¢”°¼õĀż”±»ņ”°²»±ä”±£©”£
£Ø5£©·“Ó¦“ļĘ½ŗāŗó£¬ĘäĖūĢõ¼ž²»±ä£¬Ōö¼ÓČŻĘ÷Ģå»ż£¬Ę½ŗā½«__________£ØĢī”°ÕżĻņŅĘ¶Æ”±”¢”°ÄęĻņŅĘ¶Æ”±»ņ”°²»ŅĘ¶Æ”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼ČæÉŅŌÓĆĄ“¼ų±šŅŅĻ©ŗĶ¼×Ķ飬ÓÖæÉŅŌÓĆĄ“³żČ„¼×ĶéÖŠ»ģÓŠµÄŅŅĻ©£¬µĆµ½“æ¾»µÄ¼×ĶéµÄ·½·ØŹĒ
A. Óė×ćĮæµÄäåĖ®·“Ó¦ B. Ķعż³ĪĒåŹÆ»ŅĖ® C. ĖįŠŌKMnO4ČÜŅŗ D. ÅØĮņĖį
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ŌŚ³±ŹŖµÄæÕĘųÖŠ£¬ĀķæŚĢśŗĶ°×ĢśĘ¤¶Ę²ćŹÜĖšŗó£¬Ģś¶¼±ČŹÜĖšĒ°øüČŻŅ×ÉśŠā
B. CaCO3(s) = CaO(s)£«CO2(g) ŹŅĪĀĻĀ²»ÄÜ×Ō·¢½ųŠŠ£¬ĖµĆ÷øĆ·“Ó¦µÄ¦¤H<0
C. ·“Ó¦N2(g)£«3H2(g)![]() 2NH3£Øg£©¦¤H<0“ļµ½Ę½ŗāŗó£¬ÉżøßĪĀ¶Č£¬·“Ó¦ĖŁĀŹv(H2)ŗĶH2µÄĘ½ŗā×Ŗ»ÆĀŹ¾łŌö“ó
2NH3£Øg£©¦¤H<0“ļµ½Ę½ŗāŗó£¬ÉżøßĪĀ¶Č£¬·“Ó¦ĖŁĀŹv(H2)ŗĶH2µÄĘ½ŗā×Ŗ»ÆĀŹ¾łŌö“ó
D. ŅŃÖŖĀČĘų”¢äåÕōĘų·Ö±šøśĒāĘų·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ØQ1”¢Q2µÄÖµ¾ł“óÓŚĮć£©£ŗH2(g) +Cl2(g) = 2HCl(g) ”÷H1= -Q1 kJ”¤mol-1 H2(g) +Br2(g) = 2HBr(g) ”÷H2= -Q2 kJ”¤mol-1 Ōņ”÷H1<”÷H2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚČŻ»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ“ęŌŚČēĻĀ·“Ó¦£ŗ2SO2(g)+O2(g)![]() 2SO3(g) ”÷H<O£¬Ä³ŃŠ¾æŠ”×éŃŠ¾æĮĖĘäĖūĢõ¼ž²»±äŹ±£¬øıäijŅ»Ģõ¼ž¶ŌÉĻŹö·“Ó¦µÄÓ°Ļģ£¬ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ
2SO3(g) ”÷H<O£¬Ä³ŃŠ¾æŠ”×éŃŠ¾æĮĖĘäĖūĢõ¼ž²»±äŹ±£¬øıäijŅ»Ģõ¼ž¶ŌÉĻŹö·“Ó¦µÄÓ°Ļģ£¬ĻĀĮŠ·ÖĪöÕżČ·µÄŹĒ

A. Ķ¼IŃŠ¾æµÄŹĒt0Ź±æĢŌö“óO2µÄÅØ¶Č¶Ō·“Ó¦ĖŁĀŹµÄÓ°Ļģ
B. Ķ¼IIŃŠ¾æµÄŹĒt0Ź±æĢŌö“óŃ¹Ēæŗó¶Ō·“Ó¦ĖŁĀŹµÄÓ°Ļģ
C. Ķ¼IIIŃŠ¾æµÄŹĒ“߻ƼĮ¶Ō»ÆŃ§Ę½ŗāµÄÓ°Ļģ£¬ĒŅ¼×µÄ“߻Ɗ§ĀŹ±ČŅŅøß
D. Ķ¼IIIŃŠ¾æµÄŹĒĪĀ¶Č¶Ō»ÆŃ§Ę½ŗāµÄÓ°ÉĪ£®ĒŅŅŅµÄĪĀ¶Č½Ļøß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ100 mL 6 mol”¤L£1µÄH2SO4øś¹żĮæŠæ·Ū·“Ó¦£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ£¬ŅŖĻė¼Óæģ·“Ó¦½ųŠŠµÄĖŁĀŹ£¬µ«ÓÖ²»Ó°ĻģÉś³ÉµÄĒāĘųµÄ×ÜĮ棬æÉĻņ·“Ó¦ĪļÖŠ¼ÓČėŹŹĮæµÄ
A. ŹŹĮæÅØH2SO4 B. Ķ C. “×ĖįÄĘ¹ĢĢå D. ĻõĖį¼ŲČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com