
某小组取一定质量的FeSO4固体,利用下图装置进行实验。

实验 | 实验过程 | 实现现象 |
① | 通入一段时间N2,加热 | A中固体变为红棕色,B中有白色沉淀,D试管中有无色液体 |
② | 用带有火星的木条靠近装置D的导管口 | 木条复燃 |
③ | 充分反应,停止加热,冷却后,取A中固体,加盐酸 | 固体溶解,溶液呈黄色 |
④ | 将③所得溶液滴入D试管中 | 溶液变为浅绿色 |
已知:SO2熔点-72℃,沸点-10℃;SO3熔点16.8℃,沸点44.8 ℃。
(1)实验③反应的离子方程式是_____________________________________________。
(2)分解过程除产生使木条复燃的气体外,仅由A中固体颜色变化推测,还一定有________气体,依据是____________________________________________________
(3)实验④反应的离子方程式是_____________________________________________。
(4)某同学依据B中的现象,认为FeSO4分解一定有SO3生成。你认为是否正确,并说明原因:____________________________________________(用必要的文字和化学方程式解释)。
(1)Fe2O3+6H+=2Fe3++3H2O
(2)SO2 有Fe2O3生成,在FeSO4中只有+6价S有氧化性(能被还原),因此一定有SO2生成
(3)2Fe3++SO2+2H2O=2Fe2++SO42—+4H+
(4)不正确,因为分解反应有O2和SO2生成,水溶液中发生反应:2SO2+O2+2H2O=2H2SO4,故无论分解反应是否有SO3生成,都会有此现象
【解析】加热FeSO4固体,根据实验现象及氧化还原反应知识,FeSO4分解生成Fe2O3和O2外,还有SO2生成。因为FeSO4分解生成的O2和SO2在水溶液中发生反应生成H2SO4,故无论FeSO4分解时是否有SO3产生,B中都有白色沉淀;若有SO3产生,C中的浓硫酸可吸收SO3。O2和SO2进入D中,在冰盐水混合物作用下,SO2变为无色液体,将FeCl3溶液滴入D试管中,发生反应:2Fe3++SO2+2H2O=2Fe2++SO42—+4H+。


科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题1物质的组成分类性质及化学用语练习卷(解析版) 题型:选择题
下列说法中正确的是( )。
A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同
B.某金属阳离子的结构示意图为 ,其与Cl-形成的强电解质都是离子化合物
,其与Cl-形成的强电解质都是离子化合物
C.二硫化碳是直线形非极性分子,其电子式为
D.中子数为18的氯原子可表示为18Cl
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题12化学实验基础练习卷(解析版) 题型:选择题
下列实验不能达到目的的是( )。
A.用AlCl3溶液和过量氨水制备Al(OH)3
B.用NH4Cl和Ca(OH)2固体混合加热制备NH3
C.用NaOH溶液除去苯中的溴
D.用足量铜粉除去FeCl2溶液中的FeCl3杂质
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题10常见非金属元素及其重要化合物练习卷(解析版) 题型:实验题
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性。
某兴趣小组用如图所示装置进行Mg与SO2反应的实验。

(1)选择制取SO2的合适试剂________(填编号)。
①浓HCl ②浓H2SO4 ③Na2SO3固体 ④CaSO3固体
(2)上述装置还可优化,优化的方法是________________________________________,装置C中NaOH溶液的作用是___________________________________________________________
(3)甲同学推测Mg与SO2的反应和Mg与CO2的反应相似,则该反应方程式为_________________________________________;
乙同学的推测是:2Mg+3SO2 2MgSO3+S;丙同学的推测是:3Mg+SO2
2MgSO3+S;丙同学的推测是:3Mg+SO2 2MgO+MgS,要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
2MgO+MgS,要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
已知:MgSO3和MgS都微溶于水,能与盐酸发生复分解反应放出气体;H2S气体通入CuSO4溶液中出现黑色沉淀。
限选试剂:2 mol·L-1盐酸、2 mol·L-1硝酸、蒸馏水、2 mol·L-1 NaOH溶液、品红溶液、澄清石灰水、2 mol·L-1 CuSO4溶液;仪器和用品自选。
序号 | 实验步骤 | 预期现象和结论 |
① | 取少量反应后所得固体于试管中 |
|
② | 向试管中的固体慢慢滴加____________,试管口塞上带导管的单孔塞,并将导管通入盛有________的试管中 | 若试管中的________,则丙同学推测正确,若试管中的固体未完全溶解,且________,则乙同学推测正确 |
根据上述实验探究,能证明甲同学推测正确的操作和预期现象是
_____________________________________________________________。
(4)上述实验需要100 mL 2 mol·L-1的盐酸,配制时选用________(选填10 mL、25 mL、50 mL或100 mL)量筒量取36.5%密度为1.19 g·mL-1的浓盐酸的体积为________mL。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题10常见非金属元素及其重要化合物练习卷(解析版) 题型:填空题
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl―→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是( )。
选项实验现象解释或结论
Aa处变蓝,b处变
红棕色氧化性:Cl2>Br2>I2
Bc处先变红,后褪色氯气与水生成了酸性物质
Cd处立即褪色氯气与水生成了漂白性物质
De处变红色还原性:Fe2+>Cl-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 综合实验设计练习卷(解析版) 题型:实验题
某化学学习小组设计下图实验装置(夹持装置略去)制备Cl2,并探究氯气的相关性质。

(1)若A装置中固体药品为KClO3,则反应中每生成1 mol Cl2时转移电子的物质的量为________mol。
(2)装置B既能除去氯气中的氯化氢,还能检测实验过程中装置C是否发生堵塞。若C中发生堵塞,则B中将观察到的现象是_______________________________________。
(3)装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是________、________。
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性。请简述能说明氯、溴、碘非金属性强弱的实验操作及现象:_____________________________________________。
(5)请用化学方程式说明装置F的作用:_______________________________________。
(6)甲同学提出,装置F中的试剂可改用足量的Na2SO3溶液,乙同学认真思考后认为此法不可行。请用离子方程式解释乙认为不可行的原因:_______________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 有机推断练习卷(解析版) 题型:填空题
化合物A(C12H16O2)经碱性水解、酸化后得到B和C(C8H8O2)。C中含有苯环,且苯环上有2种氢原子。B经过下列反应后得到G,G由碳、氢、氧三种元素组成,相对分子质量为172,元素分析表明,含碳55.8%,含氢7.0 %,核磁共振氢谱显示只有一个峰。

请回答下列问题:
(1)A的结构简式为_______________,G的分子式为______________。
(2)B的名称为_____________,D中官能团的名称为________________。
(3)写出F→G的化学方程式:________________________________,该反应属于_________(填反应类型)。
(4)写出满足下列条件的C的3种同分异构体的结构简式:___________________。
①是苯的对位二取代化合物;②能与FeCl3溶液发生显色反应;③不考虑烯醇( )结构。
)结构。
(5)在G的粗产物中,经检测含有聚合物杂质。写出聚合物杂质可能的结构简式(写出1种即可):_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮冲刺非选择题增分专练 化学工艺流程练习卷(解析版) 题型:填空题
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42—等杂质,提纯工艺流程如下:

Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:

Ⅱ.有关物质的溶度积如下:
物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
回答下列问题:
(1)加入NaOH溶液后过滤得到的滤渣中主要含有________(填写化学式)。25℃时,向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8 时,c(Mg2+)∶c(Fe3+)=________。
(2)操作X为________,其温度应控制在_____________________________________
(3)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行________,并说明理由______________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮专题复习 电解质溶液与电离平衡练习卷(解析版) 题型:填空题
pC类似pH,是指极稀溶液中,溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。下图为,H2CO3在加入强酸或强碱溶液后,平衡时溶液中三种成分的pC—pH图。请回答下列问题:

(1)在人体血液中,HC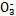 能起到使人体血液pH保持在7.35~7.45的作用。①请用电解质溶液中的平衡解释: (用离子方程式表示)。
能起到使人体血液pH保持在7.35~7.45的作用。①请用电解质溶液中的平衡解释: (用离子方程式表示)。
②正常人体血液中,HC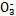 的水解程度 电离程度(填“<”“>”或“=”)。
的水解程度 电离程度(填“<”“>”或“=”)。
③pH=7.00的血液中,c(H2CO3) c(HC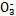 )(填“<”“>”或“=”)。
)(填“<”“>”或“=”)。
(2)H2CO3一级电离平衡常数的数值 ≈ 。
≈ 。
(3)某同学认为该溶液中Na2CO3的水解是微弱的,发生水解的C 不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确
不超过其总量的10%。请你设计简单实验证明该同学的观点是否正确
。
(4)已知某温度下Li2CO3的Ksp为1.68×10-3,将适量Li2CO3固体溶于100 mL水中至刚好饱和,饱和Li2CO3溶液中c(Li+)=0.15 mol·L-1、c(C )=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
)=0.075 mol·L-1。若t1时刻在上述体系中加入100 mL 0.125 mol·L-1 Na2CO3溶液,列式计算说明是否有沉淀产生。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com