
| A. | 与水反应可生成酸的氧化物都是酸性氧化物 | |
| B. | 既能与酸反应又能与碱反应的物质一定是两性氧化物或两性氢氧化物 | |
| C. | 晶体的熔化、水的汽化和液化、KMnO4溶液的酸化以及煤的气化和液化均属物理变化 | |
| D. | 有单质参加的反应或有单质生成的反应不一定是氧化还原反应 |
分析 A.与水反应可生成酸的氧化物不一定是酸性氧化物;
B.Al、碳酸氢铵等均与酸、碱反应;
C.煤的气化和液化属于化学变化;
D.同素异形体之间的变化没有发生氧化还原反应.
解答 解:A.酸性氧化物是和碱反应生成盐和水,中心元素化合价不变,二氧化氮和水反应生成硝酸和一氧化氮,发生氧化还原反应,中心元素氮元素发生改变,所以二氧化氮不是酸性氧化物,所以与水反应可生成酸的氧化物不一定是酸性氧化物,故A错误;
B.Al、碳酸氢铵等均与酸、碱反应,既能与酸又能与碱反应的物质可能是两性氧化物或两性氢氧化物,故B错误;
C.煤的汽化和液化过程中都有新物质的生成,属于化学变化,故C错误;
D.同素异形体之间的变化没有发生氧化还原反应,如2O3?3O2,故D正确.
故选D.
点评 本题考查氧化还原反应,为高频考点,侧重于基本概念的理解,要求学生能熟练把握物质的性质,答题时能举出实例,难度不大.


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 样品中Fe元素的质量为2.24 g | B. | 滤液A中的阳离子为Fe2+、Fe3+、H+ | ||
| C. | 样品中CuO的质量为4.0 g | D. | V=896 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
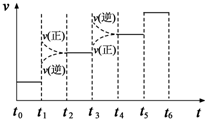 氨是一种重要的化工原料,氨的合成和应用仍是当前的重要研究内容之一.化学方程式为N2(g)+3H2(g)?2NH3(g)△H<0
氨是一种重要的化工原料,氨的合成和应用仍是当前的重要研究内容之一.化学方程式为N2(g)+3H2(g)?2NH3(g)△H<0查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 仅①② | B. | 仅①②③ | C. | 仅①②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20.0% | B. | 38.7% | C. | 50.0% | D. | 81.3% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com