
| A.常温下在水中的溶解能力:AgCl>AgBr>AgI |
| B.在AgCl饱和溶液中加入足量浓NaBr溶液有AgBr沉淀生成 |
| C.在AgBr饱和溶液中加入足量浓NaCl溶液不可能有AgCl沉淀生成 |
| D.在AgI饱和溶液中加入NaI固体有AgI沉淀析出 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.25℃时,0.lmol·L-1溶液中pH=l |
| B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中没有沉淀产生 |
| D.该体系中HF与CaC12反应产生沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小 |
| B.向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色 |
| C.将0.001 mol·L-1的AgNO3溶液滴入KCl和KI的混合溶液中,一定先产生AgI沉淀 |
| D.向AgCl的饱和溶液中加入NaCl晶体,有AgCl析出且溶液中c(Ag+)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入适量的CuSO4固体 | B.加入少量的氢氧化钠固体 |
| C.通入适量的H2S气体 | D.加入适量水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.25℃时,0.1 mol·L-1 HF溶液中pH=1 | B.Ksp(CaF2)随温度和浓度的变化而变化 |
| C.该体系中没有沉淀产生 | D.该体系中HF与CaCl2反应产生沉淀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
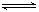 cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系:
cC(g)+dD(g)达到平衡时,各物质的物质的量浓度满足以下关系: (为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)
(为一常数),K称为化学平衡常数,它的值只与温度有关。现有反应:CO(g)+H2O(g)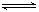 CO2(g)+H2(g),△H<0。在850℃时,K=1。
CO2(g)+H2(g),△H<0。在850℃时,K=1。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 CO(g) + H2O(g),其平衡常数K和温度t的关系如下:
CO(g) + H2O(g),其平衡常数K和温度t的关系如下:| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
 H2(g)+CO2(g) △H=-41.2kJ/mol,制备CO2与H2的混合气体。用碱液吸收一定量CO2的方法来提高混合气中H2与CO2的体积比。若以1L1.5mol/L的NaOH溶液充分吸收了22.4L(已折算为标准状况下体积)CO2,则吸收后溶液中各离子浓度从大到小的顺序是 。
H2(g)+CO2(g) △H=-41.2kJ/mol,制备CO2与H2的混合气体。用碱液吸收一定量CO2的方法来提高混合气中H2与CO2的体积比。若以1L1.5mol/L的NaOH溶液充分吸收了22.4L(已折算为标准状况下体积)CO2,则吸收后溶液中各离子浓度从大到小的顺序是 。 CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol
CO2(g)+ 2H2O(1) ΔH1=-890.3 kJ/mol  H2O(1) ΔH2=-285.8 kJ/mol
H2O(1) ΔH2=-285.8 kJ/mol 
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgI比AgCl稳定 | B.氯的非金属性比碘强 |
| C.I-的还原性比Cl-强 | D.AgI的溶解度比AgCl小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
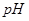 的变化如下图所示。下列判断正确的是( )
的变化如下图所示。下列判断正确的是( ) 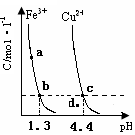
A.加适量浓NH3·H2O可使溶液由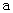 点变到 点变到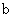 点 点 |
B.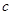  两点代表的溶液中 两点代表的溶液中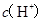 与 与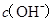 乘积不相等 乘积不相等 |
C.Cu(OH)2在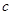 点比在d点代表的溶液中溶解程度小 点比在d点代表的溶液中溶解程度小 |
D.该温度下,氢氧化铁的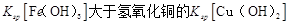 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com