
| A.13 | B.12 | C.11 | D.10 |
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.溶液的pH相同时,3种溶液物质的量浓度大小顺序是③>②>① |
| B.溶液的pH相同时,将3种溶液稀释相同倍数,pH变化最大的是① |
C.溶液的pH相同时,由水电离出的 大小顺序是③>②>① 大小顺序是③>②>① |
| D.若3种溶液的物质的量浓度都相同,则溶液的pH大小顺序是①>②>③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.c(Na+)+ c(H+)= c(OH—)+ c(HCO3—)+ 2c(CO32—) |
B.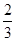 c(Na+)= c(HCO3—)+ c(CO32—)+ c(H2CO3) c(Na+)= c(HCO3—)+ c(CO32—)+ c(H2CO3) |
| C.c(Na+)> c(CO32—)> c(HCO3—)> c(OH—)> c(H+) |
| D.c(Na+)> c(HCO3—)> c(CO32—)> c(OH—)> c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在任何条件下,纯水的PH都等于7 |
| B.在任何条件下,纯水都呈中性 |
| C.在95℃时,纯水的PH大于7 |
| D.在95℃时,纯水中H+物质的量浓度小于10-7mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.③ | B.④ | C.①③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③⑤ | B.①④⑥ | C.①②④⑥ | D.①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com