
【题目】天然食用香料X是芳香族化合物,可以从某些植物中提取。由x合成H的路线如下:
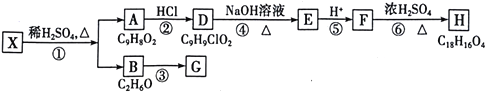
已知:①A的核磁共振氢谱有6个峰;②H为酯类物质,结构中除苯环外还含有一个六元环;③G的产量是衡量一个国家石油化工发展水平的标志。
请回答下列问题:
(1)A的结构简式为_____________________________。
(2)⑥的反应类型为___________________,反应③的化学方程式为___________________________。
(3)F中所含官能团的名称为_________________,其同分异构体中,遇FeCl3溶液发生显色反应,且能与碳酸氢钠溶液反应,其苯环上一氯代物只有一种,符合条件的同分异构体数目为______种,写出其中一种结构简式__________________________________。
(4)设计一条以G为起始原料合成乙二酸的路线________________(无机物任选,注明反应条件),示例如下:
【答案】 ![]() 取代(酯化)反应
取代(酯化)反应 ![]() 羟基、羧基 2
羟基、羧基 2 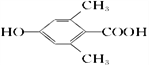 或
或 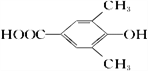 H2CCH2
H2CCH2![]() BrH2CCH2Br
BrH2CCH2Br![]() HOCH2CH2OH
HOCH2CH2OH![]() OHCCHO
OHCCHO![]() HOOCCOOH
HOOCCOOH
【解析】本题考查有机推断和合成,(1)X为酯,且B的分子式,推出B的结构简式为CH3CH2OH,G的产量是衡量一个国家石油化工发展水平的标志,则G为CH2=CH2,A为羧酸,根据A的分子式,以及A核磁共振氢谱有6个峰,X为芳香化合物,推出A为![]() ,反应②为加成反应,D的结构简式可能为
,反应②为加成反应,D的结构简式可能为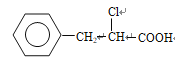 或
或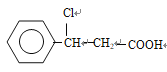 ,反应④发生中和反应和水解反应,E的结构简式可能为
,反应④发生中和反应和水解反应,E的结构简式可能为 或
或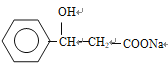 ,反应⑤是酸性强的制取酸性弱的,F的结构简式可能为
,反应⑤是酸性强的制取酸性弱的,F的结构简式可能为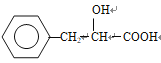 或
或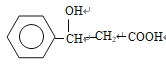 ,H为酯,结构中除苯环外还含有一个六元环,因此推出F的结构简式为
,H为酯,结构中除苯环外还含有一个六元环,因此推出F的结构简式为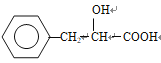 ,(1)根据上述分析,A的结构简式为
,(1)根据上述分析,A的结构简式为![]() ;(2)反应⑥为酯化反应或取代反应,反应③属于消去反应,其反应方程式为
;(2)反应⑥为酯化反应或取代反应,反应③属于消去反应,其反应方程式为![]() ;(3)根据上述分析,F中含有的官能团是羧基和羟基;遇到FeCl3溶液发生显色反应,说明含有酚羟基,能与碳酸氢钠反应,说明含有羧基,苯环上一氯代物只有一种结构,说明是对称结构,符合条件的同分异构体为
;(3)根据上述分析,F中含有的官能团是羧基和羟基;遇到FeCl3溶液发生显色反应,说明含有酚羟基,能与碳酸氢钠反应,说明含有羧基,苯环上一氯代物只有一种结构,说明是对称结构,符合条件的同分异构体为 、
、  ,共有两种;(4)乙烯先于卤素单质发生加成反应,然后在氢氧化钠的水溶液加热,发生水解反应,生成乙二醇,然后氧化乙二醇得到乙二酸,合成路线为H2CCH2
,共有两种;(4)乙烯先于卤素单质发生加成反应,然后在氢氧化钠的水溶液加热,发生水解反应,生成乙二醇,然后氧化乙二醇得到乙二酸,合成路线为H2CCH2![]() BrH2CCH2Br
BrH2CCH2Br HOCH2CH2OH
![]() OHCCHO
OHCCHO![]() HOOCCOOH。
HOOCCOOH。


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是( )
A.酸:HNO3、H2SO4、NaHSO4、HCl
B.碱性氧化物:CuO、Na2O、CaO、MgO
C.胶体:牛奶、豆浆、碘酒、氢氧化铝
D.酸性氧化物:CO2、NO、SiO2、SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.摩尔是国际科学界建议采用的一种物理量
B.HNO3的摩尔质量是63g
C.我们把含有6.02×1023个粒子的任何粒子的集体计量为1摩尔
D.1mol氧含6.02×1023个O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(都不为零),达到平衡时,X、Y、Z浓度分别为0.1 mol·L-1、0.3 mol·L-1和0.08 mol·L-1,则下列判断不合理的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(都不为零),达到平衡时,X、Y、Z浓度分别为0.1 mol·L-1、0.3 mol·L-1和0.08 mol·L-1,则下列判断不合理的是( )
A. c1∶c2=1∶3
B. 平衡时,Y和Z的生成速率之比为2∶3
C. X和Y的转化率相等
D. c1的取值范围为0<c1<0.14 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向1 L的密闭容器中加入1 mol X、0.3 mol Z和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
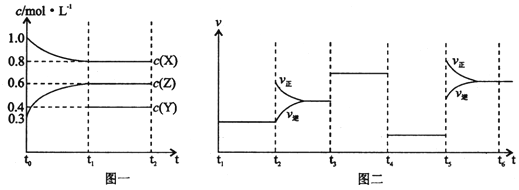
A.Y的起始物质的量为0.5 mol
B.该反应的化学方程式为:2X(g)+Y(g) ![]() 3Z(g) H<0
3Z(g) H<0
C.若t0=0,t1=10 s,则t0~t1阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
D.反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的正确组合是( )
混合物 | 氧化物 | 含氧酸 | 碱 | 盐 | |
A | 空气 | SiO2 | H2SO4 | Na2CO3 | NaHCO3 |
B | 冰水混合物 | Na2O | NaHSO4 | NaOH | NaCl |
C | 水煤气 | CuO | HCl | NH3 . H2O | CaF2 |
D | 盐酸 | Na2O2 | HNO3 | Ca(OH)2 | CaCO3 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学校实验室从化学试剂商店买回18.4 mol·L-1的硫酸。现用该浓硫酸配制
100 mL 1 mol·L-1的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有________(选填序号),还缺少的仪器有________(写仪器名称)。
(2)配制100 mL 1 mol·L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为________mL(保留一位小数),量取浓硫酸时应选用__________(选填①10 mL、②50 mL、③100 mL)规格的量筒。
(3)实验中造成所配溶液浓度偏高的原因可能是________。
A.容量瓶中原来含有少量蒸馏水
B.未经冷却,立即转移至容量瓶并洗涤烧杯,定容
C.烧杯没有洗涤
D.向容量瓶中加水定容时眼睛一直仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按酸、碱、盐分类依次排列,正确的是( )
A.硫酸、纯碱、石膏
B.硫酸、烧碱、胆矾
C.硫酸氢钠、生石灰、醋酸钠
D.磷酸、熟石灰、苛性钠
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com