��2011?����һģ�����ǵ����Ϻ�����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺
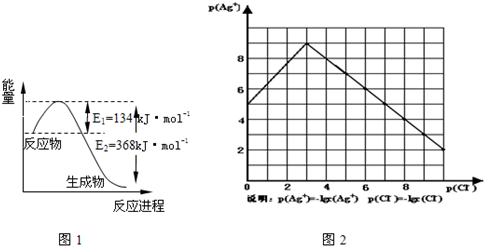
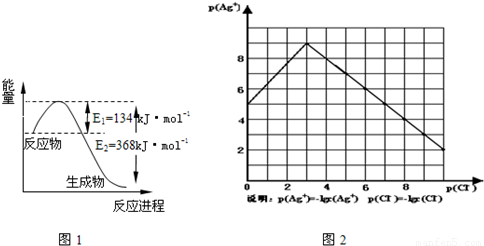
��1��ͼ1��1mol NO
2��1mol CO��Ӧ����CO
2��NO�����������仯ʾ��ͼ����д��NO
2�� CO��Ӧ���Ȼ�ѧ����ʽ
NO2��g��+CO��g���TCO2��g��+NO��g����H=-234kJ?mol-1
NO2��g��+CO��g���TCO2��g��+NO��g����H=-234kJ?mol-1
| t/�� |
200 |
300 |
400 |
| K |
K1 |
K2 |
0.5 |
��2����0.5L���ܱ������У�һ�����ĵ����������������»�ѧ��Ӧ��N
2��g��+3H
2��g��?2NH
3��g����H��0���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ�����������������⣻
���ԱȽ�K
1��K
2�Ĵ�С��K
1��
��
K
2�������������=��������
�����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������
c
c
���������ĸ��
a��������N
2��H
2��NH
3��Ũ��֮��Ϊ1��3��2 b���ԣ�N
2��������=3�ԣ�H
2�����棩
c��������ѹǿ���ֲ��� d�����������ܶȱ��ֲ���
��400��ʱ����Ӧ2NH
3��g��?N
2��g��+3H
2��g���Ļ�ѧƽ�ⳣ����ֵΪ
2
2
�������NH
3��N
2��H
2�����ʵ����ֱ�Ϊ3mol��2mol��1molʱ����÷�Ӧ��
�ԣ�N
2��������
��
��
�ԣ�N
2�����棩 ����д����������=������=��
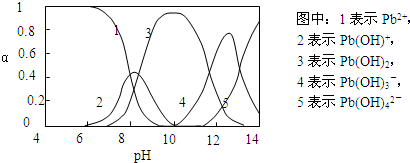
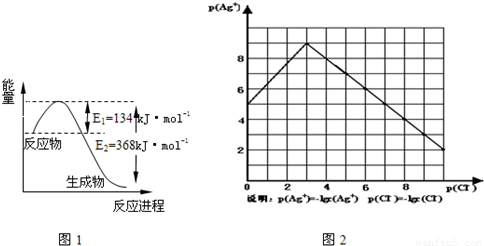
�����ﲢ�Ǿ��Բ��ܣ�����ˮ�����ֲ�ͬ����Һ���ܽ��������ͬ��ͬ����ЧӦ�����
����γɵȶ���ʹ��������ܽ�������ı䣮��֪AgCl+Cl
-�T[AgCl
2]
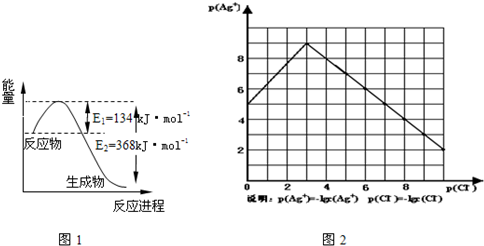
-��ͼ2��ij�¶���AgCl��NaCl��Һ�е��ܽ������
��������Ϣ��֪��
��1����ͼ֪���¶���AgCl���ܶȻ�����Ϊ
10-12
10-12
��
��2��AgCl��NaCl��Һ�е��ܽ������ͼ��ʾ������ȱ�С����ԭ���ǣ�
Cl-������AgCl���ܽ⣬��Cl-Ũ������ʹAgCl�γ�����AgCl+Cl-�T[AgCl2]-
Cl-������AgCl���ܽ⣬��Cl-Ũ������ʹAgCl�γ�����AgCl+Cl-�T[AgCl2]-
��3�����ʵ��֤��S��AgCl����S��AgI����S��Ag
2S����ʵ�鷽����
��AgCl����Һ�еμ�KIϡ��Һ��0.1mol/L���������ɰ�ɫת��Ϊ��ɫ����������Һ�еμ�ͬŨ��Na2Sϡ��Һ��0.1mol/L���������ɻ�ɫת��Ϊ��ɫ
��AgCl����Һ�еμ�KIϡ��Һ��0.1mol/L���������ɰ�ɫת��Ϊ��ɫ����������Һ�еμ�ͬŨ��Na2Sϡ��Һ��0.1mol/L���������ɻ�ɫת��Ϊ��ɫ
��
��4������AgCl�γɵ���Һ�еμӰ�ˮ��ʲô����
��ɫ�����ܽ⣬�γ���ɫ��Һ
��ɫ�����ܽ⣬�γ���ɫ��Һ
��������Ӧ�����ӷ���ʽΪ
AgCl+2NH3=Ag��NH3��2++Cl-
AgCl+2NH3=Ag��NH3��2++Cl-
��



 ��������������������ϵ�д�
��������������������ϵ�д�
 2NH3��g��
2NH3��g�� [N2H5?H2O]++H+
[N2H5?H2O]++H+ [N2H5?H2O]++H+
[N2H5?H2O]++H+