
| A、2NO+O2=2NO2 |
| B、N2+O2=2NO |
| C、N2+3H2=2NH3 |
| D、3NO2+H2O=2HNO3+NO |
科目:高中化学 来源: 题型:
 Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液(加入一定量酸),示意图如图所示.该电池工作时,下列说法正确的是( )
Mg-H2O2电池可用于驱动无人驾驶的潜航器.该电池以海水为电解质溶液(加入一定量酸),示意图如图所示.该电池工作时,下列说法正确的是( )| A、Mg电极是该电池的正极 |
| B、电池总反应为Mg+H2O2+2H+═Mg2++2H2O |
| C、电池工作时,石墨周围海水的pH减少 |
| D、电池工作时,溶液中的H+向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、正极被保护 |
| B、H+向Zn电极移动 |
| C、加入少量KSCN溶液,变血红色 |
| D、负极的电极反应式是:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.5mol/L |
| B、2.0mol/L |
| C、1.0mol/L |
| D、3.0mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③⑤ |
| C、②④⑤ | D、④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
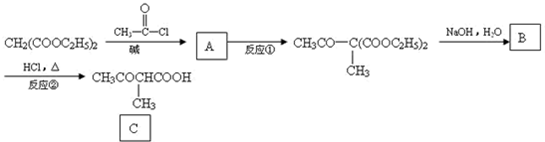
| ①D |
| 碱 |
| ②NaOH,H2O |
| ③HCl,△ |
 COOH,
COOH,查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com