
分析 (1)依据热化学方程式和盖斯定律计算得到所需热化学方程式;
(2)根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡;根据三行式以及化学平衡常数表达式计算化学平衡常数;
(3)①依据平衡常数随温度变化,平衡常数越大,平衡正向进行,温度越高平衡向吸热反应方向进行;
②分析判断反应是放热反应,反应物能量高于生成物,焓变是反应物和生成物之间的能量差值与变化过程无关;
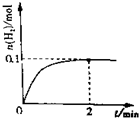
(4)某温度时,根据H2浓度随时间的变化曲线,氢气浓度减小到平衡不变,甲醇浓度增大到平衡不变,依据物质的量的变化绘出CH2OH浓度随时间的变化曲线.
解答 解:(1)2 I2(s)+5O2(g)=2 I2O5(s);△H=-75.56kJ•mol-1①,
2CO(g)+O2(g)=2 CO2(g);△H=-566.0kJ•mol-1②,
将方程式②×$\frac{5}{2}$-①×$\frac{1}{2}$得5CO(g)+I2O5(s)=5 CO2(g)+I2(s);△H=(-566.0kJ•mol-1)×$\frac{5}{2}$-(-75.56kJ•mol-1)×$\frac{1}{2}$=-1377.22kJ/mol,
所以其热化学反应方程式为:5CO(g)+I2O5(s)=5 CO2(g)+I2(s)△H=-1377.22kJ/mol,
故答案为:5CO(g)+I2O5(s)=5 CO2(g)+I2(s)△H=-1377.22kJ/mol;
(2)本反应是反应前后气体分子数不变的反应,故体系的压强保持不变,故a不能说明反应已达到平衡状态;随着反应的进行,NO2的浓度减小,颜色变浅,故b可以说明反应已达平衡;SO3和NO都是生成物,比例保持1:1,故c不能作为平衡状态的判断依据;d中所述的两个速率都是逆反应速率,不能作为平衡状态的判断依据,故选b;
NO2(g)+SO2(g)?SO3(g)+NO(g)
起始物质的体积 a 2a 0 0
转化物质的体积 x x x x
平衡物质的体积 a-x 2a-x x x
则(a-x):(2a-x)=1:6,故x=$\frac{4}{5}$a,故平衡常数为=$\frac{{x}^{2}}{(a-x)(2a-x)}$=$\frac{8}{3}$.
故答案为:b;$\frac{8}{3}$;
(3)反应方程式为CO(g)+2H2(g)?CH3OH(g)
①该反应在40℃和60℃时的平衡常数分别为K1和K2,若K1大于K2,说明温度升高平衡常数减小,平衡逆向进行,正反应是放热反应;
故答案为:放热;
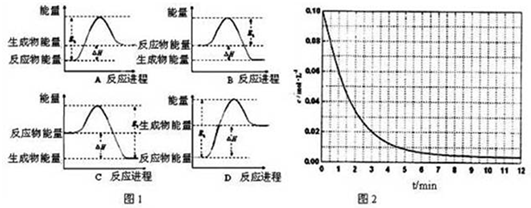
②反应是放热反应,反应物能量高于生成物,焓变是反应物和生成物之间的能量差值;
A、反应物能量低于生成物反应是吸热反应,故A错误;
B、反应物能量高于生成物是放热反应,焓变符合,活化能是正反应的活化能,故B正确;
C、反应物能量高于生成物是放热反应,焓变符合,活化能不是正反应的活化能,故C错误;
D、反应物能量低于生成物反应是吸热反应,故D错误;
故答案为:B;
(4)某温度时,根据图象中的H2浓度随时间的变化曲线,氢气浓度减小到平衡不变,甲醇浓度增大到平衡不变,依据氢气的浓度和化学方程式计算甲醇浓度的增加描点画出图象,(0.01,0.02)(0.02,0.04)(0.03,0.06),(0.04,0.08)绘出CH2OH浓度随时间的变化曲线为: ;故答案为:
;故答案为: .
.
点评 本题考查了热化学方程式和盖斯定律计算应用,化学平衡影响因素的分析判断,化学平衡的计算应用,图象分析绘制,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 空气中的污染物主要来源为燃煤、机动车尾气等.因此,CO、SO2、NOx等进行研究具有重要意义.请回答下列问题:
空气中的污染物主要来源为燃煤、机动车尾气等.因此,CO、SO2、NOx等进行研究具有重要意义.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
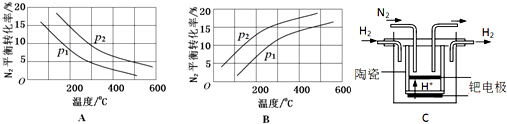
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 时间/min | 0 | 10 | 20 | 30 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
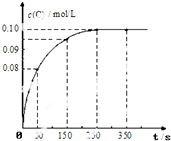 在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )
在一定温度下,向2L恒容密闭容器中充入1mol A,发生A(g)?B(g)+C(g)反应.反应过程中c(C) 随时间变化的曲线如图所示,下列说法不正确的是( )| A. | 反应在0~50s的平均速率v(C)=1.6×10-3mol/(L•s) | |
| B. | 该温度下,反应的平衡常数K=0.025 | |
| C. | 保持其他条件不变,升高温度,平衡时c(B)=0.11mol/L,则该反应的△H<0 | |
| D. | 反应达平衡后,再向容器中充入 1 mol A,该温度下再达到平衡时0.1mol/L<c(C)<0.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
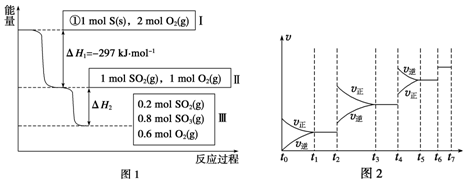
| t1~t2 | t3~t4 | t5~t6 | t6~t7 |
| K1 | K2 | K3 | K4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com