
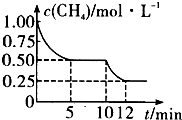
 在密闭容器中进行反应CH4(g)+H20(g)?CO(g)+3H2(g)△H>0测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )
在密闭容器中进行反应CH4(g)+H20(g)?CO(g)+3H2(g)△H>0测得c(CH4)随反应时间(t)的变化如图所示.下列判断正确的是( )| A、10 min时,改变的外界条件可能是温度 |
| B、0~5 min内,V(H2)=0.1 mol?L-1?min-1 |
| C、恒温下,缩小容器体积,平衡后c(H2)肯定减小 |
| D、10-12 min时反应的平衡常数逐渐增大 |
| △c |
| △t |
| 1mol/L-0.5mol/L |
| 5min |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 h后反应进行完全,容器中的N2浓度为0.55 mol?L-1 |
| B、前20 min用NH3表示的反应速率为0.01 mol?L-1?min-1 |
| C、增加H2的浓度或降低温度,平衡将向正反应方向移动,且反应速率均加快 |
| D、当容器内压强不改变时,说明反应已达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、它的中子数是118 |
| B、它是第八周期元素 |
| C、它是活泼的金属元素 |
| D、它的最外层电子数是8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
时间(min) | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |

查看答案和解析>>
科目:高中化学 来源: 题型:
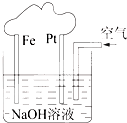
| A、这是一个电解池装置 |
| B、这是电解NaOH溶液的装置 |
| C、该装置中Fe为阴极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
| D、该装置中Pt为正极,电极反应为:O2+2H2O+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三个烧杯中一定均会发生的离子反应有:2Na+2H2O=2Na++2OH-+H2↑ |
| B、三个烧杯中钠均在液面上剧烈反应,相比而言,X烧杯中的反应平缓些 |
| C、Z烧杯中一定会有沉淀生成,但沉淀不是单质铜 |
| D、三个烧杯中置换生成气体的物质的量一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O3和O2互为同位素 |
| B、O3比O2稳定 |
| C、等质量的O3和O2含有相同的原子数 |
| D、O3与O2的相互转变是物理变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com