
| A. | 1mol的任何气体中都含有6.02×1023个分子 | |
| B. | 12g12C中含有6.02×1023个碳原子 | |
| C. | 1mol水中含有6.02×1023个氢原子 | |
| D. | 物质的量相等的CO和CO2所含的C原子个数也相等 |
分析 根据n=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$结合物质的构成计算.
解答 解:A.1mol气体含有阿伏伽德罗常数个分子,约为6.02×1023,故A正确;
B.12C的摩尔质量为12g/mol,则12g12C的物质的量为1mol,含有6.02×1023个碳原子,故B正确;
C.1mol水中含有2mol H原子,则含有2×6.02×1023个氢原子,故C错误;
D.CO和CO2分子中都含有1个C原子,则物质的量相等的CO和CO2所含的C原子个数也相等,故D正确.
故选C.
点评 本题综合考查物质的量的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用以及相关概念的理解,难度不大.


科目:高中化学 来源: 题型:解答题
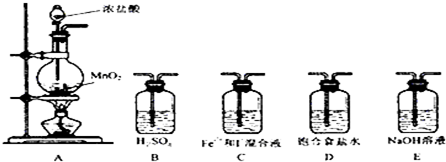
| 实验步骤 | 预期现象与结论 |
| 取少量反应的溶液置于A、B两支试管中; 向A试管中滴加KSCN; 向B试管中滴加淀粉: | ①若A变红色, B不变色则假设1成立 ②若A不变色, B变蓝色则假设2成立 ③若A变红色, B变蓝色则假设3成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
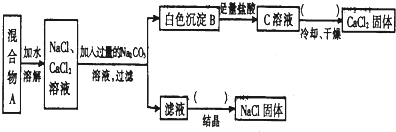
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝热反应,化学方程式为2Fe+Al2O3═2Al+Fe2O3 | |
| B. | 原电池是电能转化为化学能的装置 | |
| C. | 绿色植物的光合作用则实现了光能向化学能的转化 | |
| D. | 氯碱工业用电解饱和食盐水来制备氯气和火碱就是将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知A、B、C、D、X、Y是原子序数依次增大的前20号元素,其中A~D的原子序数 是连号的,A的基态原子有3个不同的能级,各能级中的电子数相等;X和Y位于同一主族,
已知A、B、C、D、X、Y是原子序数依次增大的前20号元素,其中A~D的原子序数 是连号的,A的基态原子有3个不同的能级,各能级中的电子数相等;X和Y位于同一主族,查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓硫酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气的摩尔质量是71 g/mol | |
| B. | 通过树状分类法可把硝酸和硫酸分入强酸,把纯碱分入正盐 | |
| C. | 酸性的雨水都是酸雨,酸雨的PH小于7 | |
| D. | 1mol CO2的质量是44 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )
某反应由两步反应A?B?C构成,它的反应能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列有关叙述正确的是( )| A. | A→C的反应为吸热反应 | B. | 三种物质中B最不稳定 | ||
| C. | 加入催化剂,E1、E2、E3、E4均不变 | D. | A→C反应的△H=E1-E2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com