
| A、A、B、C的浓度相等 |
| B、容器中压强不再变化 |
| C、单位时间消耗nmol A,同时生成2n mol C |
| D、A、B、C的分子数比为1:3:2 |


科目:高中化学 来源: 题型:
| A、加入少量氢氧化钠 |
| B、加入少量盐酸 |
| C、加入少量水 |
| D、加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽油、柴油和植物油都属于烃 |
| B、乙醇既能被氧化为乙醛也能被氧化为乙酸 |
| C、乙烯和苯加入溴水中,都能观察到褪色现象,原因是都发生了加成反应 |
| D、淀粉和纤维素互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、废纸、金属、玻璃、塑料属于可回收利用垃圾 |
| B、空气质量报告中涉及的污染物主要是SO2、NO2和可吸入颗粒物 |
| C、应用离子交换树脂既可以软化硬水,又可杀菌消毒 |
| D、装饰材料是居室空气污染的源头之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=1溶液中:K+、Mg2+、AlO2-、S2O32- | ||
| B、Na2S溶液中:SO42-、K+、Cl-、Cu2+ | ||
C、
| ||
| D、含Fe2+溶液中:Na+、ClO-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L己烷中共价键数目为19NA | ||
B、1L浓度为1mol?L-1的Na2CO3溶液中含有NA个CO
| ||
C、1cm3铁所含的铁原子数是
| ||
| D、常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、SO42-、Na+、SiO32- |
| B、Ag+、Fe3+、Cl-、SO42- |
| C、K+、SO42-、Mg2+、NO3- |
| D、H+、I-、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
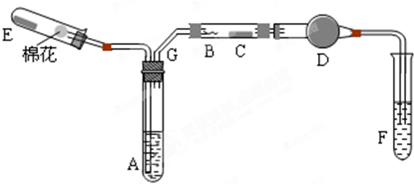
查看答案和解析>>
科目:高中化学 来源: 题型:
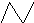 ,有机物A的键线式结构为
,有机物A的键线式结构为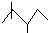 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.则:
,有机物B与等物质的量的H2发生加成反应可得到有机物A.则:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com