
| A.H2(g)的燃烧热△H=-285.8 kJ/mol,则2H2O(g)=2H2(g)+O2(g)△H=+571.6 kJ/mol |
| B.反应物的总能量低于生成物的总能量时,该反应为放热反应 |
| C.由石墨比金刚石稳定可知:c(金刚石,s)=c(石墨,s)△H<0 |
D.已知:298K时,N2(g)+3H2(g) 2NH3(g)△H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入1/2 mol N2和3/2 mol H2,达到平衡时放出46.0 kJ的热量 2NH3(g)△H=-92.0 kJ/mol。在相同温度下,向密闭容器中通入1/2 mol N2和3/2 mol H2,达到平衡时放出46.0 kJ的热量 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题

| A.图①表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B.图②表示0.1000 mol·L-1NaOH溶液滴定20.00mL 0.1000 mol·L-1HCl溶液所得到的滴定曲线 |
| C.图③表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |
| D.图④表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③④ | B.①③⑤ | C.①②④⑤ | D.②⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.反应前盐酸溶液的温度 | B.反应前盐酸溶液的质量 |
| C.反应前氢氧化钠溶液的温度 | D.反应前氢氧化钠溶液的质量 |
| 实验 序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
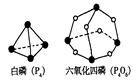
| A.+1638KJ·mol–1 | B.–1638KJ·mol–1 | C.+126KJ·mol–1 | D.–126KJ·mol–1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.煤可以通过汽化或液化后再燃烧以提高燃烧效率 |
| B.电池工作时将化学能转变成电能 |
| C.绿色植物光合作用过程中太阳能转变成化学能 |
| D.生物质能只能通过含有生物质能的物质的直接燃烧转化成热能从而被利用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.灼热的碳和二氧化碳的反应 | B.Ba (OH)2 .8H2O晶体和NH4Cl晶体混合 |
| C.氢氧化钠和硫酸的反应 | D.CaCO3分解 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.锌与硫酸反应制取氢气 | B.高温条件下碳粉与二氧化碳的反应 |
| C.高温煅烧石灰石 | D.Ba(OH)2·8H2O晶体与NH4Cl固体反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com