
【题目】如图所示是实验室蒸馏石油的实验装置,实验需要收集60~150℃和150~300℃的馏分。请回答下列问题:
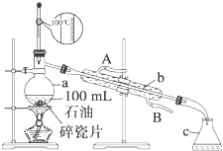
(1)仪器a的规格和名称_______,仪器b、c的名称:b_______,c_______。
(2)实验所选温度计是错误的,正确的选择应该是_______。
(3)实验时在仪器a中加入了少量碎瓷片,其目的是_______。
(4)实验时在仪器b中通入冷却水,请指明冷却水的流向_______。
科目:高中化学 来源: 题型:
【题目】为消除目前燃料燃烧时产生的环境污染,同时缓解能源危机,有关专家提出了利用太阳能制取氢能的构想。下列说法正确的是:
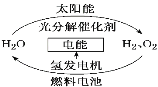
A. H2O的分解反应是放热反应
B. 氢能源已被普遍使用
C. 2 mol液态H2O具有的总能量低于2 mol H2和1 mol O2的能量
D. 氢氧燃料电池放电过程中是将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:乙烯产量是衡量一个国家石油化工水平的主要标志。下图是由乙烯合成乙酸乙酯可能的合成路线:
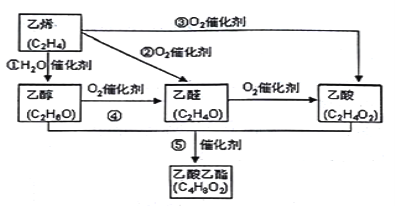
请回答下列问题:
(1)反应④的化学方程式为_____________________________ ;
(2)在实验室制备乙酸乙酯时,用到饱和的碳酸钠溶液,其作用是:___________________;
(3)乙醇的结构式为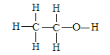 ,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 _________________________________;
,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 _________________________________;
Ⅱ:酸奶中含有乳酸,乳酸在常温常压下是一种无色的粘度很大的液体。取9.0g乳酸与足量的Na反应,在标准状况下可收集到2.24L气体;另取9.0g乳酸与足量的NaHCO3溶液反应,生成的CO2气体在标准状况下体积为2.24L。已知乳酸分子中含有一个甲基,请回答下列问题:
(1)乳酸的相对分子质量为:_______________________;
(2)在浓硫酸存在的条件下,两分子乳酸相互反应生成环状酯类化合物,请写出该反应的化学反应方程式:________________________,其反应类型为:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 1mol 的P4O6中含有6 NA个P—O键
B. 0.1mo1H2和0.1molI2于密闭容器中充分反应后,分子总数小于0.2 NA
C. pH=3的CH3COOH溶液中,含有10-3NA个H+
D. 高温下,16.8gFe 与足量的水蒸气反应,失去0.8NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及化学学科观点的有关说法正确的是![]()
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,一种烷烃A和一种单烯烃B组成混合气体,A 或B 分子均最多只含有4 个碳原子,且B 分子的碳原子数比A 分子的多。将1升该混合气体充分燃烧,在同温同压下得到2.5升CO2气体。120℃时取1 升该混合气体与9 升氧气混和,充分燃烧后,当恢复到120℃和燃烧前的压强时,体积增大6.25%。则A 和B 的分子式分别为( )
A. C2H6、C4H8 B. C2H6、C3H6
C. CH4、C4H8 D. CH4、C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O===O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
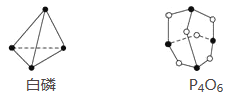
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃的锌锰干电池对环境污染很大,工业上可用如下工艺回收正极材料中的金属(部分条件未给出):
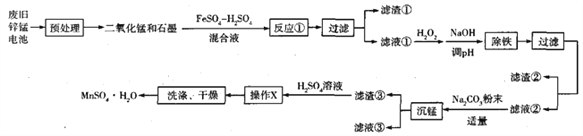
(1)废弃的锌锰干电池对环境的主要危害是__________, ![]() 中
中![]() 的化合价为__________。
的化合价为__________。
(2)锌锰干电池中氯化铵为电解质,其电子式为______________________________。
(3)反应①中氧化剂与还原剂的物质的量之比为______________________________。
(4)该工艺流程中多次用到过滤,实验室中过滤所需要的玻璃仪器有__________。
(5)已知:25℃时, ![]() ,滤液①中加入NaOH溶液至pH=_________时,
,滤液①中加入NaOH溶液至pH=_________时, ![]() 沉淀完全
沉淀完全![]() 时,认为
时,认为![]() 沉淀完全]。
沉淀完全]。
(6)写出“沉锰”过程中生成碱式碳酸锰![]() 的离子方程式为:______________________________________________________________________。
的离子方程式为:______________________________________________________________________。
(7)用硫酸酸化的![]() 浆液可吸收工业废气中的
浆液可吸收工业废气中的![]() 生成
生成![]() ,已知浆液中
,已知浆液中![]() 含量为
含量为![]() ,工业废气中
,工业废气中![]() 含量为
含量为![]() ,
, ![]() 的吸收率可达90%,则处理1000
的吸收率可达90%,则处理1000![]() 工业尾气,可得到
工业尾气,可得到![]() 的质量为__________kg(用含字母的代数式表示)。
的质量为__________kg(用含字母的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com