
不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,x越大,其原子吸引电子的能力越强。下面是某些短周期元素的x值:
| 元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
| x值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 |
(1)通过分析x值变化规律,确定Mg的x值范围:____<x(Mg)<________。
(2)推测x值与原子半径的关系是________________________________________________;
根据短周期元素的x值变化特点,体现了元素性质的________________变化规律。
(3)分别指出下列两种化合物中氧元素的化合价:HClO________,HFO________。
(4)经验规律告诉我们:成键的两原子相应元素x数值的差值为Δx,当Δx>1.7时,一般为离子键,当Δx<1.7时,一般为共价键,试推断AlBr3中化学键类型是________________。
(5)预测元素周期表中,x值最小的元素位于第________周期第________族(放射性元素除外)。
答案 (1)0.9 1.5 (2)同周期(同主族)中,x值越大,其原子半径越小 周期性 (3)-2 0 (4)共价键 (5)六 ⅠA
解析 (1)x代表电负性的大小,根据位置关系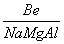 判断x(Na)<x(Mg)<x(Be),即0.9<x(Mg)<1.5。
判断x(Na)<x(Mg)<x(Be),即0.9<x(Mg)<1.5。
(2)x值越大,其原子半径越小,电负性随着原子序数的递增,呈现周期性变化。
(3)根据电负性的数值,在HClO中氧为-2价,根据
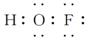 ,H和O的共用电子对偏向O,而O和F的共用电子对又偏向F,所以O为0价。
,H和O的共用电子对偏向O,而O和F的共用电子对又偏向F,所以O为0价。
(4)x(Br)-x(Al)<x(Cl)-x(Al)=3.0-1.5=1.5,所以AlBr3中化学键类型为共价键。
(5)电负性最小的应为金属性最强的。


科目:高中化学 来源: 题型:
用标准盐酸溶液滴定未知浓度的NaOH溶液(酚酞作指示剂),用“偏高”、“偏低”或“无影响”填空。
(1)酸式滴定管未用标准溶液润洗( )
(2)锥形瓶用待测溶液润洗( )
(3)锥形瓶洗净后还留有蒸馏水( )
(4)放出碱液的滴定管开始有气泡,放出液体后气泡消失( )
(5)酸式滴定管滴定前有气泡,滴定终点时气泡消失( )
(6)部分酸液滴出锥形瓶外( )
(7)酸式滴定管滴定前读数正确,滴定后俯视读数(或前仰后俯)( )
(8)酸式滴定管滴定前读数正确,滴定后仰视读数(或前俯后仰)( )
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2 080 | 4 000 | 6 100 | 9 400 |
| R | 500 | 4 600 | 6 900 | 9 500 |
| S | 740 | 1 500 | 7 700 | 10 500 |
| T | 580 | 1 800 | 2 700 | 11 600 |
| U | 420 | 3 100 | 4 400 | 5 900 |
(1)在周期表中,最可能处于同一族的是________。
A.Q和R B.S和T C.T和U D.R和T
E.R和U
(2)下列离子的氧化性最弱的是________。
A.S2+ B.R2+ C.T3+ D.U+
(3)下列元素中,化学性质和物理性质最像Q元素的是________。
A.硼 B.铍 C.氦 D.氢
(4)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明:________________________________________________________________________,
如果U元素是短周期元素,你估计它的第2次电离能飞跃数据将发生在失去第______个电子时。
(5)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是__________,其中________元素的第一电离能异常高的原因是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现代大爆炸理论认为:天然元素源于氢、氦等发生的原子核融合反应。这与100多年前,普鲁特运用思辨性推测作出“氢是所有元素之母”的预言恰好“一致”。下列说法正确的是 ( )
A.科学研究中若能以思辨性推测为核心,就能加快科学的进程
B.普鲁特“既然氢最轻,它就是其他一切元素之母”的推理是符合逻辑的
C.“一致”是巧合,普鲁特的预言没有科学事实和理论支撑,它只是一种猜测
D.“现代大爆炸理论”是解释宇宙诞生的唯一正确的理论
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组原子中,化学性质一定相似的是 ( )
A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子
B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子
C.2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子
D.最外层都只有一个电子的X、Y原子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于极性键的叙述中不正确的是( )
A.是由不同元素原子形成的共价键
B.共价化合物中必定存在极性键
C.极性键中电负性大的原子显正电性
D.共用电子对必然偏向吸引电子能力强的原子一方
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH3COOH??CH3COO-+H+达到电离平衡时,电离平衡常数可以表示为Ka= ;CH3COO-+H2O??CH3COOH+OH-达到水解平衡时,水解平衡常数可以表示为Kh=
;CH3COO-+H2O??CH3COOH+OH-达到水解平衡时,水解平衡常数可以表示为Kh= (式中各粒子浓度均为平衡时浓度)。
(式中各粒子浓度均为平衡时浓度)。
(1)对于任意弱电解质来讲,其电离平衡常数Ka、对应离子的水解常数Kh以及水的离子积常数Kw的关系是______________________,由此可以推断,弱电解质的电离程度越小,其对应离子的水解程度____________。
(2)由于CH3COOH的电离程度很小,计算时可将CH3COOH的平衡浓度看成是CH3COOH溶液的浓度,则c mol·L-1的CH3COOH溶液中c(H+)=________(不为0)。
(3)现用某未知浓度(设为c′)的CH3COOH溶液及其他仪器、药品,通过实验测定一定温度下CH3COOH的电离平衡常数,需测定的数据有(用简要的文字说明):
①实验时的温度;
②________________________________________________________________________;
③用____________(填一种实验方法)测定溶液浓度c′。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解质的说法中正确的是( )
A.强电解质一定是离子化合物
B.强电解质、弱电解质的电离一般都是吸热过程
C.强电解质的饱和溶液一定是浓溶液
D.强电解质在水中一定能全部溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com