
| A. | 常温下,0.1mol•L-1的CH3COOH溶液中,由水电离出的c(H+)为1.0×10-13mol•L-1 | |
| B. | pH=2与pH=1的CH3COOH溶液中c(H+)之比为1:10 | |
| C. | 常温下,等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液的pH<7 | |
| D. | 25℃时,完全中和50mLpH=3的H2SO4溶液,需要pH=11的NaOH溶液50mL |
分析 A.醋酸是弱电解质存在电离平衡,0.1mol•L-1的CH3COOH溶液中氢离子浓度小于0.1mol•L-1;
B.pH=2的醋酸溶液中c(H+)=10-2mol/L,pH=1的CH3COOH溶液中c(H+)=10-1mol/L;
C.醋酸是弱酸存在电离平衡,常温下,等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,醋酸又电离出氢离子,溶液显酸性;
D.强酸强碱完全中和反应氢离子物质的量和氢氧根离子物质的量相同.
解答 解:A.醋酸是弱电解质存在电离平衡,0.1mol•L-1的CH3COOH溶液中氢离子浓度小于0.1mol•L-1,由水电离出的c(H+)大于1.0×10-13mol•L-1 ,故A错误;
B.pH=2的醋酸溶液中c(H+)=10-2mol/L,pH=1的CH3COOH溶液中c(H+)=10-1mol/L,pH=2与pH=1的CH3COOH溶液中c(H+)之比=10-2:10-1=1:10,故B正确;
C.醋酸是弱酸存在电离平衡,常温下,等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,醋酸又电离出氢离子,溶液显酸性,常温下,等体积pH=12的NaOH溶液和pH=2的CH3COOH溶液混合,混合后溶液的pH<7,故C正确;
D.25℃时,完全中和50mLpH=3的H2SO4溶液中氢离子物质的量n(H+)=0.050L×10-3mol/L=5×10-5mol/L,pH=11的NaOH溶液50mL中氢氧根离子物质的量n(OH-)=$\frac{1{0}^{-14}}{1{0}^{-11}}$mol/L×0.050L=5×10-5mol/L,氢离子物质的量和氢氧根离子物质的量相同强酸强碱完全中和反应,故D正确;
故选A.
点评 本题考查了酸碱溶液中PH计算、弱电解质电离平衡的分析应用、主要是离子积常数和电离平衡的判断,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 将碳块磨成粉末可加快反应速率 | |
| B. | 增加碳的质量可加快反应速率 | |
| C. | 升高温度可加快反应速率 | |
| D. | 容器体积不变时,向容器中充入氦气,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强碱性溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 含有大量NH4+的溶液:Mg2+、S2-、OH-、I- | |
| C. | 通有足量NO2的溶液:K+、Na+、SO32-、AlO2- | |
| D. | 强酸性溶液中:Na+、Fe3+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Al3+、SO42-、NO3- | B. | K+、Na+、ClO-、NH4+ | ||
| C. | K+、NH4+、MnO4-、SO42- | D. | Na+、K+、NO3-、HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和C(金刚石) | B. | CO2和H2 | C. | NaCl和HCl | D. | MgCl2和KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
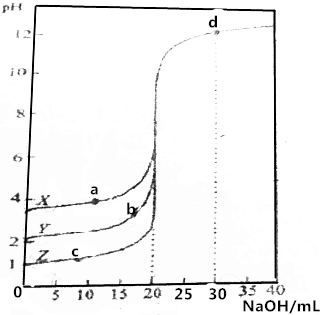 用0.1000mol•L-1的NaOH溶液分别滴定0.1000mol•L-1、20.00mLX、Y、Z三种酸溶液.溶液pH与加入NaOH体积之间的关系如图所示,下列说法错误的是( )
用0.1000mol•L-1的NaOH溶液分别滴定0.1000mol•L-1、20.00mLX、Y、Z三种酸溶液.溶液pH与加入NaOH体积之间的关系如图所示,下列说法错误的是( )| A. | Z为一元强酸 | |
| B. | d点的c(OH-)为0.02000mol•L-1 | |
| C. | a、b、c中b点的阴离子的物质的量浓度最大 | |
| D. | X、Y为一元弱酸,且其电离常数:Ka(x)<Ka(Y) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 燃烧是发光、发热的化学反应 | B. | 燃烧必须有02参加 | ||
| C. | 燃烧必须有H20参加 | D. | 燃烧一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
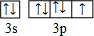 ,R基态原子的外围电子排布式为3d104s1.
,R基态原子的外围电子排布式为3d104s1.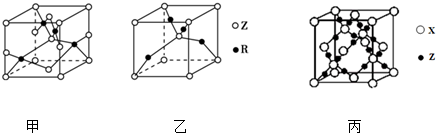
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com