
| A£® | ¶¼¾ßÓŠĪüĖ®ŠŌ | |
| B£® | Ā¶ÖĆÓŚæÕĘųÖŠ¶¼ÄÜŠĪ³É°×Īķ | |
| C£® | Ā¶ÖĆÓŚæÕĘųÖŠ£¬ČÜŅŗÅØ¶Č¾ł½µµĶ | |
| D£® | ŌŚæÕĘųÖŠ³¤ĘŚĀ¶ÖĆ£¬ČÜŅŗÖŹĮæ¾ł¼õĒį |
·ÖĪö A£®ÅØĻõĖį²»¾ßÓŠĪüĖ®ŠŌ£»
B£®ÅØĮņĖįÄѻӷ¢£¬ÅØĻõĖįŅ×»Ó·¢£»
C£®ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬ÅØĻõĖį¾ßÓŠ»Ó·¢ŠŌ£»
D£®ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬ÅØĻõĖįŅ×»Ó·¢£¬¾Ż“Ė½ā“š£®
½ā“š ½ā£ŗA£®ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬ÅØĻõĖį²»¾ßÓŠĪüĖ®ŠŌ£¬¹ŹA“ķĪó£»
B£®ÅØĮņĖįÄѻӷ¢£¬Ā¶ÖĆÓŚæÕĘųÖŠ²»»įÉś³É°×Īķ£¬ÅØĻõĖįŅ×»Ó·¢£¬Ā¶ÖĆÓŚæÕĘųÖŠ»įÉś³É°×Īķ£¬¹ŹB“ķĪó£»
C£®Ā¶ÖĆÓŚæÕĘųÖŠ£¬ÅØĻõĖį»Ó·¢£¬ÅØĮņĖį¾ßÓŠĪüĖ®£¬ČÜŅŗÅØ¶Č¾ł½µµĶ£¬¹ŹCÕżČ·£»
D£®ÅØĮņĖį¾ßÓŠĪüĖ®ŠŌ£¬Äܹ»ĪüŹÕæÕĘųÖŠµÄĖ®¶ųŹ¹ČÜŅŗÖŹĮæŌö¼Ó£¬ÅØĻõĖįŅ×»Ó·¢£¬ČÜÖŹ¼õÉŁ£¬ČÜŅŗÖŹĮæ¼õŠ”£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗC£®
µćĘĄ ±¾Ģāæ¼²éÅØĻõĖįŗĶÅØĮņĖįµÄŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕÅØĖįµÄĒæŃõ»ÆŠŌ”¢ÅØĮņĖįµÄČż“óĢŲŠŌĪŖ½ā“šµÄ¹Ų¼ü£¬×¢ÖŲ»ł“”ÖŖŹ¶µÄ漲飬ĢāÄæÄŃ¶Č²»“ó£®


 øߊ§ÖĒÄÜæĪŹ±×÷ŅµĻµĮŠ“š°ø
øߊ§ÖĒÄÜæĪŹ±×÷ŅµĻµĮŠ“š°ø ½Ż¾¶ŃµĮ·¼ģ²ā¾ķĻµĮŠ“š°ø
½Ż¾¶ŃµĮ·¼ģ²ā¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³äµē¹ż³ĢŹĒ»ÆѧÄÜ×Ŗ»ÆĪŖµēÄܵĹż³Ģ | |
| B£® | ³äµēŹ±Ńō¼«·“Ó¦ĪŖCd£ØOH£©2+2e-ØTCd+2OH - | |
| C£® | ·ÅµēŹ±µē³ŲÄŚ²æOH-ĻņÕż¼«ŅĘ¶Æ | |
| D£® | ³äµēŹ±ÓėÖ±Į÷µēŌ“Õż¼«ĻąĮ¬µÄµē¼«ÉĻ·¢ÉśNi£ØOH£©2×Ŗ»ÆĪŖNiO£ØOH£©µÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ÆŗĻ·“Ó¦ | B£® | ·Ö½ā·“Ó¦ | C£® | ÖĆ»»·“Ó¦ | D£® | ø“·Ö½ā·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŖĖŲÖÜĘŚ±ķÓŠ7øöÖ÷×å7øöÖÜĘŚ | |
| B£® | Ō×Ó×īĶāµē×Ó²ćÖ»ÓŠ2øöµē×ÓµÄŌŖĖŲæÉÄÜŹĒ½šŹōŌŖĖŲŅ²æÉÄÜŹĒ·Ē½šŹōŌŖĖŲ | |
| C£® | ŌŚŌŖĖŲÖÜĘŚ±ķÖŠĪ»ÓŚ½šŹōŌŖĖŲŗĶ·Ē½šŹōŌŖĖŲ½»½ē“¦×īČŻŅ×ÕŅµ½ÄĶøßĪĀÄĶøÆŹ“µÄŗĻ½š²ÄĮĻ | |
| D£® | ŌŖĖŲÖÜĘŚ±ķÖŠ“Ó¢óB×åµ½¢ņB×å10øöׯŠŠµÄŌŖĖŲ¶¼ŹĒ½šŹōŌŖĖŲ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
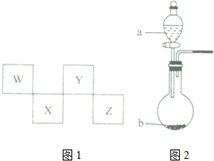 W”¢X”¢Y”¢ZĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼1ĖłŹ¾£¬ĘäÖŠYÓėÄĘŌŖĖŲŗĶĒāŌŖĖŲ¾łæÉŠĪ³ÉŌ×ÓøöŹż1£ŗ1ŗĶ1£ŗ2µÄ»ÆŗĻĪļ£®
W”¢X”¢Y”¢ZĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼1ĖłŹ¾£¬ĘäÖŠYÓėÄĘŌŖĖŲŗĶĒāŌŖĖŲ¾łæÉŠĪ³ÉŌ×ÓøöŹż1£ŗ1ŗĶ1£ŗ2µÄ»ÆŗĻĪļ£®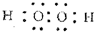 £¬ZŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖƵŚČżÖÜĘŚ¢÷A×壮
£¬ZŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖƵŚČżÖÜĘŚ¢÷A×壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
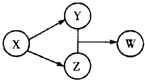 X”¢Y”¢Z”¢WĖÄÖÖĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦ĪļŗĶ²śĪļŅŃ¾Ź”ĀŌ£©£®ĻĀĮŠ×éŗĻÖŠ²»·ūŗĻøĆ¹ŲĻµµÄŹĒ
X”¢Y”¢Z”¢WĖÄÖÖĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø²æ·Ö·“Ó¦ĪļŗĶ²śĪļŅŃ¾Ź”ĀŌ£©£®ĻĀĮŠ×éŗĻÖŠ²»·ūŗĻøĆ¹ŲĻµµÄŹĒ | A | B | C | D | |
| X | HCl | Na2O2 | Na2CO3 | Al2O3 |
| Y | FeCl2 | NaOH | CO2 | AlCl3 |
| Z | Cl2 | Na2CO3 | CaCO3 | NaAlO2 |
| W | FeCl3 | NaHCO3 | Ca£ØHCO3£©2 | Al£ØOH£©3 |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
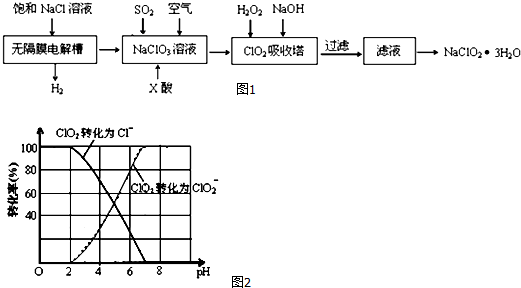
 ŅŌ°±×÷ĪŖČ¼ĮĻµÄ¹ĢĢåŃõ»ÆĪļ£Øŗ¬ÓŠ02-£©Č¼ĮĻµē³Ų£¬¾ßÓŠČ«¹ĢĢ¬½į¹¹”¢ÄÜĮ抧ĀŹøß”¢ĪŽĪŪČ¾µČĢŲµć£¬ĮķĶā°±Ęųŗ¬ĒāĮæøߣ¬²»ŗ¬Ģ¼£¬Ņ×Ņŗ»Æ£¬·½±ćŌĖŹäŗĶÖü“ę£¬ŹĒŗÜŗƵÄĒāŌ“ŌŲĢ壮Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£ŗ
ŅŌ°±×÷ĪŖČ¼ĮĻµÄ¹ĢĢåŃõ»ÆĪļ£Øŗ¬ÓŠ02-£©Č¼ĮĻµē³Ų£¬¾ßÓŠČ«¹ĢĢ¬½į¹¹”¢ÄÜĮ抧ĀŹøß”¢ĪŽĪŪČ¾µČĢŲµć£¬ĮķĶā°±Ęųŗ¬ĒāĮæøߣ¬²»ŗ¬Ģ¼£¬Ņ×Ņŗ»Æ£¬·½±ćŌĖŹäŗĶÖü“ę£¬ŹĒŗÜŗƵÄĒāŌ“ŌŲĢ壮Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com