
| A. | 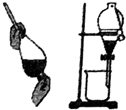 可用于分离苯和水的混合物 | |
| B. | 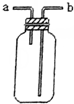 可用于收集H2、NH3、CO2、Cl2、HCl等气体 | |
| C. | 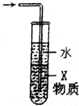 X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 | |
| D. | 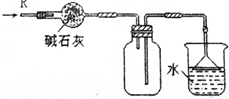 可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
分析 A.苯和水的混合物分层;
B.a进气可收集密度比空气密度小的气体,b进气可收集密度比空气密度大的气体;
C.X若为四氯化碳,可隔绝气体和水;
D.HCl与碱石灰反应,且密度比空气的密度大.
解答 解:A.苯和水的混合物分层,则可利用分液漏斗分离,故A正确;
B.a进气可收集H2、NH3等气体,b进气可收集CO2、Cl2、HCl等气体,故B正确;
C.X若为四氯化碳,可隔绝气体和水,则可用于吸收氨气或氯化氢,并防止倒吸,故C正确;
D.HCl与碱石灰反应,且密度比空气的密度大,则干燥及收集均不合理,故D错误;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离方法、气体的收集及实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | B. | 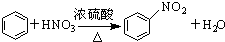 | ||
| C. | 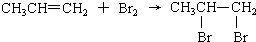 | D. | HCl+AgNO3═AgCl↓?+HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | T/K | 锌规格 | 盐酸浓度/mol•L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究锌规格(粗、细)对该反应速率的影响. |
| ② | 298 | |||
| ③ | 308 | |||
| ④ | 298 |
| 时间(s) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 氢气体积 (mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
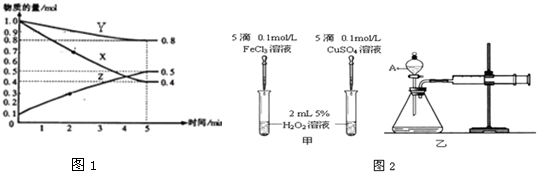
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类化合物都具有相同的官能团 | |
| B. | 糖类是提供能量最高的营养物质 | |
| C. | 蛋白质的水解产物都含有羧基和氨基 | |
| D. | 酯类在碱性条件下的水解反应称为皂化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 编号 | 0.01mol•L-1酸性KMnO4溶液 | 0.1mol•L-1 H2C2O4溶液 | 水 | 反应温度/℃ | 反应时间/s |
| ① | 5.0mL | 5.0mL | 0 | 20 | 125 |
| ② | V1 | V2 | 2.0mL | 20 | 320 |
| ③ | 5.0mL | 5.0mL | 0 | 50 | 30 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+2NH3+H2O═(NH4)2SO3 | |
| B. | NO2+NO+2NaOH═2NaNO2+H2O | |
| C. | Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O | |
| D. | CuO+H2SO4(稀)═CuSO4+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
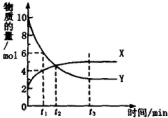
| A. | 反应的化学方程式为5Y?X | |
| B. | t1时,Y的浓度是X浓度的1.5倍 | |
| C. | t2时,正、逆反应速率相等,达到化学平衡 | |
| D. | t3时,逆反应速率大于正反应速率 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上月考一化学卷(解析版)) 题型:填空题
今有①CH3COOH ②HCl ③H2SO4三种溶液。根据要求回答下列问题:
(1)当它们pH相同时,其物质的量浓度最大的是 (填序号)
(2)当它们的物质的量浓度相同时,其pH最小是 (填序号)
(3)将c(H+)相同的三种酸均加水稀释至原来的10倍,c(H+)由大到小的顺序为 (填序号)。
(4)体积和物质的量浓度均相同的①②③三种酸溶液,分别与相同浓度的烧碱溶液恰好完全反应,所需烧碱的体积比为 ;此时所得到的三种溶液的pH大小关系为 .
(5)若酸性FeCl2废液中c(Fe2+)=2.0×10-2mol·L-1, c(Fe3+)=1.0×10-3mol·L-1, c(-)=5.3×10-2mol·L-1,则该溶液的PH约为 。
(6)FeCl3可做净水剂,净水原理是 (用离子方程式表达),FeCl3溶液中的离子浓度从大到小顺序是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com