
用如下图所示装置可以完成一系列实验(图中夹持装置已略去)
请回答下列问题:
I.(1)仪器p的名称是_________________,若用装置A由浓硫酸和亚硫酸钠固体制取SO2气体,并通过装置B完成表中设计实验,请填写表中空白:
| B中棉花的位置 | ① | ② | ③ |
| 所蘸试剂 | 石蕊试液 | 品红溶液 | 碘水(黄色) |
| 现象 | | 褪色 | |
| 体现SO2的性质 | 水溶液显酸性 | | |
I.(1)分液漏斗(1分)现象 变红(1分) 褪色(1分) 体现SO2的性质 漂白性(1分) 还原性(1分)
(2)SO2+I2+2H2O=SO42-+4H++2I- (2分)
II.(1)2Fe 2++Cl2=2Fe3++2Cl- (2分)
(2)先变红后褪色(1分) (3)氢氧化钠(NaOH)溶液 (1分)
解析试题分析:I.(1)图中仪器p为分液漏斗;SO2溶于水生成H2SO3显酸性,所以石蕊变红;SO2使品红褪色,体现了SO2的漂白性;SO2通入碘水中,SO2被I2氧化,所以碘水褪色,体现了SO2的还原性。
(2)SO2、H2O与I2反应生成HI和H2SO4,HI和H2SO4为强电解质,拆成离子可得离子方程式。
II.(1)Cl2把FeCl2氧化为FeCl3,把FeCl2和FeCl3改写为离子可得离子方程式。
(2)Cl2与H2O反应生成HCl和HClO,显酸性使石蕊变红,HClO具有强氧化性,能漂泊石蕊,所以石蕊先变红后褪色。
(3)Cl2能与强碱溶液反应,所以用NaOH溶液吸收Cl2。
考点:本题考查基本仪器、实验现象的观察与分析、离子方程式的书写、尾气的吸收。


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案科目:高中化学 来源: 题型:实验题
下图5个装置都是中学化学中常见的实验装置,某学习小组的同学欲用这些装置进行常见物质的制取并探究其性质(图中a、b、c表示止水夹),请对其进行完善或评价,试回答下列问题: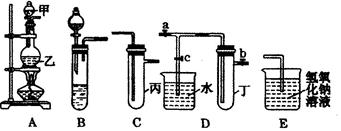
(1)将A、C、E相连后,以浓盐酸和 (填写名称)为原料制取Cl2,仪器乙的名称是 。
(2)利用(1)中装置和药品,在丙中加入适量水,即可制得氯水。将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将所得氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 向所得氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应至少产生一种酸性强于碳酸的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
浓硫酸有强氧化性,铁在冷的浓硫酸中能发生钝化。某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。请你协助他们探究所得气体的成分。
Ⅰ【提出猜想】
猜想1:所得气体中可能是SO2。 猜想2:所得气体中可能是__________。
猜想3:所得气体中可能是_______的混合气体。
Ⅱ【实验探究】
(1)将所得气体通入如下装置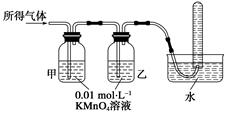
证明猜想3正确的实验现象是___________、______________、________________。
(2)点燃余下的气体前,必须要进行的操作是_________________________________。
(3)写出浓硫酸表现出强氧化性的化学反应方程式_____________________________。
(4)如果把一定量的铁与浓硫酸加热时产生的气体通过装有过量Na2O2粉末的玻璃管,则玻璃管中反应的生成物可能含有(填化学式)__________________ ___________ _。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1)仪器a的名称为________;仪器b中可选择的试剂为________;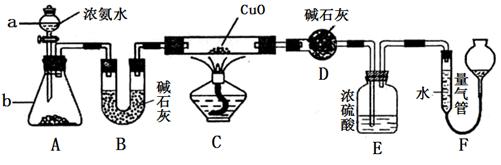
(2)实验室中利用下列各组物质,进行喷泉实验,不能成功的是( )
| A.Cl2与饱和食盐水 | B.CO2 与40%的NaOH溶液 |
| C.NH3与饱和食盐水 | D.HCl与水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某研究性学习小组设计实验方案来研究稀硝酸与铜反应生成NO。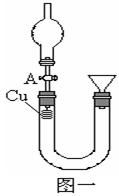
(1)补充完成下列实验步骤:
①__________________________________________;
②打开活塞A,往U型管右侧漏斗中注入稀硝酸,一直注到稀HNO3接触到A处橡皮塞为止;
③关闭活塞A,观察实验现象。
(2)记录描述观察到的实验现象:
可观察到的现象有:U型管左侧铜丝逐渐溶解,有_____色气体产生,溶液呈______色,随着反应不断进行,最后反应自行停止,该过程反应的离子方程式为________________________________。
(3)试管内装有NO,倒置于水槽中,当向试管内通入21mLO2时,最后试管中的液面仍在原来的位置,则原试管中NO的体积为_________mL。
(4)0.1L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.1mol/L和0.4mol/L。若向该混合液中加入足量的铜粉,则最多能溶解铜粉的质量_______g。若要使溶液中的Cu2+全部转化为Cu(OH)2沉淀,应加入2 mol·L-1的氢氧化钠溶液 _mL。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
为了证实木炭和浓H2SO4的反应产物,可用下列流程进行验证(箭头表示气体的流向)。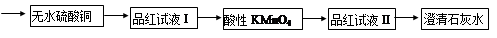
回答下列问题:
根据上述流程中什么现象证明产物是H2O、CO2、SO2:
; ; 。
(2)酸性KMnO4溶液的作用是 ,能否用溴水代替酸性高锰酸钾溶液? 。(填“能”或“不能”),请写出化学反应方程式 (若回答不能,则此空不用答题)
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1) 仪器a的名称为________;仪器b中可选择的试剂为________;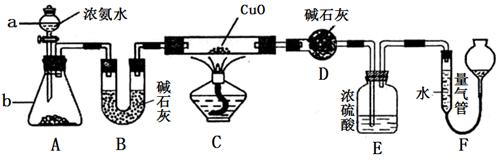
(2)实验室中利用下列各组物质,进行喷泉实验,不能成功的是 。
| A.Cl2与饱和食盐水 | B.CO2 与40%的NaOH溶液 |
| C.NH3与饱和食盐水 | D.HCl与水 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
|
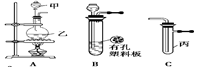
 请按要求填空:
请按要求填空:| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入 NaHCO3粉末 | 有无色气泡产生 | 氯气与水反应的产物具有较强的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知X、Y、Z、W均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物已略)。下列说法不正确的是( )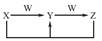
| A.X、Y、Z中至少有一种相同的元素,该元素可以是金属元素也可以是非金属元素 |
| B.物质W可能是化合物,也可能是单质 |
| C.上述转化关系中不可能出现置换反应 |
| D.若X、Y、Z中均含有一种常见金属元素,则W可能是强酸也可能是强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com