
在同温同压下,下列各组热化学方程式中,Q2>Q1的是()
A. 2H2(g)+O2(g)=2H2O(g)△H=﹣Q1kJ/mol;
2H2(g)+O2(g)=2H2O(g))△H=﹣Q2kJ/mol
B. S(g)+O2(g)=SO2(g)△H=﹣Q1kJ/mol;
S(s)+O2(g)=SO2(g))△H=﹣Q2kJ/mol
C. C(s)+ O2(g)=CO2(g))△H=﹣Q1kJ/mol;
O2(g)=CO2(g))△H=﹣Q1kJ/mol;
C(s)+O2(g)=CO(g))△H=﹣Q2kJ/mol
D. H2(g)+Cl2(g)=2HCl(g)△H=﹣Q1kJ/mol;
 H2(g)+Cl2(g)=HCl(g))△H=﹣Q2kJ/mol
H2(g)+Cl2(g)=HCl(g))△H=﹣Q2kJ/mol
考点: 反应热的大小比较.
专题: 化学反应中的能量变化.
分析: A、液态水变为气态水的过程要吸收能量;
B、固体硫燃烧时要先变为气态硫,过程吸热;
C、一氧化碳是碳单质不完全燃烧的产物,完全燃烧时生成二氧化碳,完全燃烧放热更多;
D、热化学方程式中,物质的量越多,伴随的能量变化越大.
解答: 解:A、两个反应时都是氢气和氧气生成水,但第一个式子是生成气体,第二个是液态,从气态变为液态还要放出一定的热量,所以Q2>Q1,故A正确;
B、固体硫燃烧时要先变为气态硫,过程吸热,气体与气体反应生成气体比固体和固体反应生气气体产生热量多,故B错误;
C、可以很容易地判断出来第一个是完全燃烧反应,第二个是不完全燃烧反应,那么放出的热量很明显是完全燃烧比不完全燃烧放出的多,所以Q2<Q1,故C错误;
D、反应的能量变化和反应中各物质的量成正比,故 Q2= Q1,故D错误.
Q1,故D错误.
故选A.
点评: 本题考查反应热的大小比较,题目难度中等,本题注意比较反应热的角度,化学反应中,反应的程度、物质的量以及物质的聚集状态不同,反应放出或吸收的热量是不同的.


科目:高中化学 来源: 题型:
X、Y、Z为三种气体.把 a molX和 b molY充入一密闭容器中.发生反应X+2Y⇌2Z 达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为()
A. [ ]×100% B. [
]×100% B. [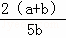 ]×100% C. [
]×100% C. [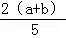 ]×100% D. [
]×100% D. [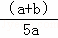 ]×100%
]×100%
查看答案和解析>>
科目:高中化学 来源: 题型:
禁止使用兴奋剂是奥运会保证运动员比赛公平的重要举措之一.以下两种兴奋剂结构分别为:

则关于它们的说法中正确的是( )
A. 利尿酸分子中有三种官能团
B. 两种分子中的所有碳原子均不可能共平面
C. 两种兴奋剂均属于芳香烃
D. 两种分子均可发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、E五种元素中,X原子核外的M层中有2个单电子且与Z同主族,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大.请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)YZ2分子的立体结构是 ;
(3)Q的元素符号是 ,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)E的氢化物的熔沸点比同族其它元素氢化物的熔沸点都要高很多,原因是 HF分子间存在
.
查看答案和解析>>
科目:高中化学 来源: 题型:
在相同条件下,下列三个化学反应放出的热量分别以△H1、△H2、△H3表示:
(1)2H2(g)+O2(g)═2H2O(g)△H1
(2)2H2(g)+O2(g)═2H2O(l)△H2
(3)H2(g)+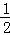 O2(g)═H2O(g)△H3
O2(g)═H2O(g)△H3
则△H1、△H2和△H3的关系是()
A. △H1=△H2=△H3 B. △H1<△H2,△H3=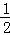 △H1
△H1
C. △H1>△H2,△H2=2△H3 D. 无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
CH3﹣CH3→CH2=CH2+H2,有关化学键的键能如下:
化学键 C﹣H C=C C﹣C H﹣H
键能(kJ/mol) 414.4 615.3 347.4 435.3
计算该反应的反应热. kJ/mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然无法直接测得,但可通过间接的方法测定.现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=﹣24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=﹣47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
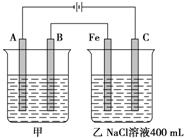
如图所示,甲、乙为相互串联的两电解池.
(1)甲池若为用电解原理精炼铜的装置,则A电极名称为阴极,电极材料是 ,电极反应式为 ,电解质溶液可以是 .
(2)乙池中Fe极电极反应式为 ,若在乙池中滴入少量酚酞试液,开始电解一段时间,Fe极附近呈 色.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com