
科目:高中化学 来源: 题型:阅读理解
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中σ键与π键数目比为1:2 | 阳离子就是一个质子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
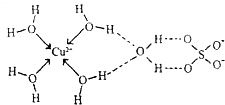 第四周期元素的单质及化合物在工农业生产中应用广泛.
第四周期元素的单质及化合物在工农业生产中应用广泛.| 元素 | Mn | Fe | |
| 电离能kJ.mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
查看答案和解析>>
科目:高中化学 来源:2009年山东省高考理综化学模拟题3 题型:022
A物质的化学式为XY2,X、Y为元素周期表前三周期的元素,其阳离子和阴离子电子层结构相同,且1 mol XY2含有30 mol电子.请回答下列问题:
(1)X基态原子的核外电子排布式为________,A物质的化学式________.
(2)元素D、E同周期,D原子的最外层电子数是其电子层数的3倍,D与Y相邻,则D的离子结构示意图是________;E原子的最外层电子数是其电子层数的2倍,D与E形成非极性分子,该分子的结构式为________.
(3)W为短周期元素,且与E同主族,其单质是________晶体;DW形成的晶体的化学式是______________.
(4)Y的氢化物能用于刻蚀玻璃,Y2与NaOH溶液反应的产物之一是OY2,该反应的离子方程式为________.
查看答案和解析>>
科目:高中化学 来源:2014届四川省绵阳市高三第一次诊断性考试理综化学试卷(解析版) 题型:填空题
已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大,X基态原子的核外电子分布在3 个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和。另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,请回答下列问题。
(1)微粒XZ32-的中心原子杂化类型为 化合物YW3的空间构型为 。
(2)R基态原子的电子排布式为 ,元素X、Y、Z的第一电离能由大到小的顺序为
(用元素符号表示)。
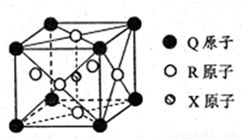
(3)一种新型导体晶体的晶胞如右图所示,则该晶体的化学式为 ,其中一个Q原子紧邻 个R原子。
(4)R的氢氧化物能溶于含XY-离子的溶液生成一种配离子[R(XY)4]2-,该反应的离子方程式是 弱酸HXY分子中存在的σ键与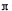 键的数目之比为
。
键的数目之比为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com