
【题目】
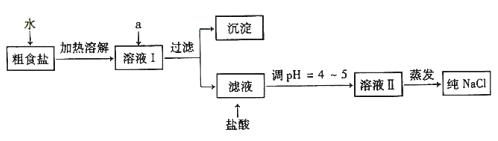
⑴粗食盐常含有少量Ca2+、Mg2+、SO42-等杂质离子,实验室提纯 NaCl 的流程如下:
提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH 溶液、Ca(OH)2溶液、BaCl2溶液、Ba(NO3)2溶液、稀盐酸、稀硫酸、AgNO3溶液。
①欲除去溶液Ⅰ中的 Ca2+、Mg2+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为_________(填化学式)。
②过滤之前,怎样检验SO42-已除去:___________。
⑵现需要480mL1.00mol·L-1NaCl溶液。
①欲配制上述溶液,则所用玻璃仪器中除过滤操作涉及到的外,还需___________。
②计算后,需称 NaCl的质量为___________。
③下列操作的正确顺序是(用字母表示) B→_______→______→_______→_______→_______→G 。
A上下颠倒摇匀 B称量 C洗涤 D定容 E溶解 F移液 G装瓶
④下列操作对所得溶液浓度有何影响,在横线上填写“偏高”、“偏低”或“无影响”。
A.称量时砝码生锈:__________; | B.溶解前烧杯内有水:__________; |
C.容量瓶洗涤后未干燥___________; | D.定容时仰视容量瓶刻度线:___________。 |
【答案】⑴①NaOH、BaCl2、Na2CO3/BaCl2、NaOH、Na2CO3/BaCl2、Na2CO3、NaOH;
②取样于试管中,先滴加足量盐酸酸化,再滴加氯化钡溶液,观察是否产生白色沉淀,未产生则证明已除净,产生则证明未除净。
⑵①500mL容量瓶,胶头滴管,量筒。
②29.3g
③B→E→F→C→D→A→G
④A.偏高;B.无影响;C.无影响;D.偏低;
【解析】试题分析:(1)①要除去SO42-,只有选BaCl2溶液,若选用Ba(NO3)2,会引入新的离子NO3-,再选用NaOH溶液除去Mg2+和Fe3+溶液,最后选用Na2CO3溶液除去Ca2+,此处不能选用K2CO3溶液,否则会引入新的K+,再用HCl除去过量的CO32-,Na2CO3溶液不能加在BaCl2溶液前,否则会引入Ba2+,故答案为:BaCl2、NaOH、Na2CO3;
②取少量待测液于试管中,向其中滴加氯化钡溶液,看是否有沉淀生成,若没有沉淀,则硫酸根离子已沉淀完全,故答案为:取少量待测液于试管中,向其中滴加氯化钡溶液,看是否有沉淀生成,若没有沉淀,则硫酸根离子已沉淀完全;
(2)①用提纯的NaCl配制480mL 1.00molL-1NaCl溶液,需要的玻璃仪器有烧杯,玻璃棒、500ml容量瓶、胶头滴管、量筒;因此还需要500ml容量瓶、胶头滴管、量筒;故答案为:500ml容量瓶、胶头滴管、量筒;
②配制500mL 1.00molL-1NaCl溶液中溶质物质的量=0.50L×1.00mol/L=0.5mol,氯化钠质量=0.5mol×58.5g/mol=29.25g;但托盘天平只能称量到0.1g,所以需要称量氯化钠质量29.3g,故答案为:29.3;
③溶液配制步骤是计算、称量、溶解、转移、洗涤转移,加水定容、摇匀、装瓶;所以操作的正确顺序是B→E→F→C→D→A→G,故答案为;B→E→F→C→D→A→G;
④A.称量时砝码生锈,砝码质量增大,称量氯化钠质量增大,结果偏高;故答案为:偏高;
B.溶解前烧杯内有水,不影响溶质的物质的量,也不影响溶液的体积,对结果无影响,故答案为:无影响;
C.容量瓶洗涤后未干燥,不影响溶质的物质的量,也不影响溶液的体积,对结果无影响,故答案为:无影响;
D.定容时仰视容量瓶刻度线,分析依据是刻度定液面,仰视加水超过刻度线,浓度偏低;故答案为:偏低。


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法错误的是
A.可用铝槽密闭盛装浓硫酸
B.工业上利用蛋白质的水解反应生产肥皂和甘油
C.乙醇可用作汽车燃料
D.食醋可用于消除暖水瓶中的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中发生反应N2+3H22NH3,经一段时间后NH3的物质的量增加了2.4mol,这段时间内用氢气表示的反应速率为0.6mol/(L.s),则这段时间为( )
A.6s B.4s C.3s D.2s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)如图所示的仪器中配制溶液肯定不需要的是_______________(填序号),配制上述溶液还需用到的玻璃仪器是____________(填仪器的名称)。
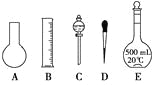
(2)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液 |
B.贮存溶液 |
C.测量容量瓶规格以下的任意体积的液体 |
D.准确稀释某一浓度的溶液 |
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.1 mol/L(填“大于”、“等于”或“小于”,下同)。若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度________0.1 mol/L。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为________mL(计算结果保留一位小数)。如果实验室有15 mL、20 mL、50 mL量筒,应选用________mL量筒最好。配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾严重影响人们的生活与健康。某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如下的实验:

已知:3NO3-+ 8Al + 5OH- + 2H2O![]() 3NH3↑+ 8AlO2-
3NH3↑+ 8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是
A.试样中肯定存在NH4+、Mg2+、SO42-和NO3-
B.试样中可能存在Na+、Cl-
C.试样中一定不含Al3+
D.该雾霾中可能存在NaNO3、NH4Cl和MgSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于食品添加剂的叙述错误的是( )
A. 亚硝酸钠是一种致癌物质 B. 营养强化剂也是一种食品添加剂
C. 醋可同时用作调味剂和防腐剂 D. 胡萝卜素和柠檬黄是常见的着色剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产生活中应用广泛,请解决下列问题。
(1)硫酸铜溶液时白磷引起中毒的一种解毒剂:
P4+CuSO4+H2O![]() Cu3P+H3PO4+H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为 。
Cu3P+H3PO4+H2SO4,若6molH3PO4生成,则被CuSO4氧化的P4的物质的量为 。
(2)氮的化合物合成、应用及氮的固定一直是科学研究的热点。以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47 kJ·mol-1
②NH2CO2NH4(s)=CO (NH2)2(s)+H2O(g);ΔH=a kJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98 kJ·mol-1
则a为 。
(3)右图表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式 。生产中可分离出的物质A的化学式为 。
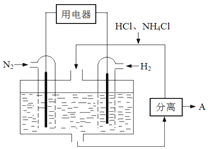
(4)常温下,向0.1mol/L氨水中加入少许N2O5,使溶液中c(NH3·H2O):c(NH4+)=5:9,此时溶液的pH= .(25℃时,NH3·H2O的电离常数Kb=1.8×10-5)
(5)SiO2溶于氢氟酸后生成一种极强的二元酸和水,经分析该酸由3种元素组成,其中氟元素的质量分数为79.17%。请写出SiO2溶于氢氟酸的离子方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com