
�ҹ��Ǹ��������,���������������һλ,��¯��������Ϊ�ձ������������ij�ֿ�ʯ����Ԫ����������FemOn����ʽ����,�ֽ�������ʵ��:����������ʯ��Ʒ����,��ȡ25.0 g��Ʒ���ձ���,����ϡ�������ܽ�,�����ϼ��ȡ�����,��ȥ�������������Һ�м���10.0 gͭ�۳�ַ�Ӧ����ˡ�ϴ�ӡ������ʣ�����3.6 g��ʣ����Һ��2 mol��L-1������KMnO4�ζ�,���յ�ʱ����KMnO4��Һ���25.0 mL��
(1)���������ʯ����Ԫ�ص�����������
(2)����������FemOn�Ļ�ѧʽ(m��nΪ������)��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ij��Һ�н����±������е�5�����ӣ�������ˮ�ĵ��뼰���ӵ�ˮ�⣩���Ҹ����ӵ����ʵ�������ȶ�Ϊ0��0lmol��
������ԭ��Һ�м���KSCN��Һ�������Ա仯��
������ԭ��Һ�м������������,���������ɣ���Һ������������䡣
������ԭ��Һ�м���BaCl2��Һ���а�ɫ�������ɡ�
�Իش���������
��1��������ԭ��Һ���ȼ�����������ᣬ�ټ���KSCN��Һ��������__________________���ù������漰�����ӷ���ʽ��________________��__________________��
��2����ԭ��Һ�м���������NaOH��Һ����ַ�Ӧ���ˡ�ϴ�ӡ����գ��������ù���Ϊ____________________��д��ѧʽ����
��3����ԭ��Һ�м����������������ˮ���ռ������������岢ʹ����ǡ�ó���������������������ˮ���У�����������ͨ��___________mLO2�����������ָ��״��������ʹ��Һ������������
��amolCu2S��bmol FeSͶ�뵽v L c mol��L��ϡ�����У���ַ�Ӧ������NO���壬���ó�����Һ���Կ���Cu��NO3��2��Fe��NO3��3��H2SO4�Ļ����Һ����Ӧ��δ����ԭ����������ʵ���Ϊ ___________mol����ͬʱ����a��b��v��c�ı���ʽ��ʾ����
����֪CH4��g����2O2��g�� CO2��g����2H2O��l�� ��H1��a kJ��mol�����㷴ӦCH4��g����4NO��g��
CO2��g����2H2O��l�� ��H1��a kJ��mol�����㷴ӦCH4��g����4NO��g�� 2N2��g����CO2��g����2H2O��l�����ʱ��H2������Ҫ����ij��Ӧ���ʱ��H3������Ӧ�и����ʻ�ѧ������֮��Ϊ���������ʱ��H3��b kJ��mol����÷�Ӧ���Ȼ�ѧ����ʽΪ______________________________________��
2N2��g����CO2��g����2H2O��l�����ʱ��H2������Ҫ����ij��Ӧ���ʱ��H3������Ӧ�и����ʻ�ѧ������֮��Ϊ���������ʱ��H3��b kJ��mol����÷�Ӧ���Ȼ�ѧ����ʽΪ______________________________________��
�ݴ˼������H2��_____________kJ��mol���ú�a��b��ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
���������һ�ֵ��͵�ǿ��������
���������գ�
������KMnO4������Һ����Cu2S��CuS�Ļ����ʱ�������ķ�Ӧ���£�
�� MnO4��+ Cu2S + H+�� Cu2+ + SO2�� + Mn2+ + H2O(δ��ƽ)
�� MnO4��+ CuS + H+ �� Cu2+ + SO2�� + Mn2+�� H2O(δ��ƽ)
��1�����й��ڷ�Ӧ�ٵ�˵���д������ ��ѡ���ţ���
a����������Ԫ����Cu��S
b���������뻹ԭ�������ʵ���֮��Ϊ8:5
c������2.24 L(�����) SO2��ת�Ƶ��ӵ����ʵ�����0.8 mol
d����ԭ�Ե�ǿ����ϵ�ǣ� Mn2+> Cu2S
��2�������Ӧ���е���ת�Ƶķ������Ŀ�� MnO4��+ CuS
����ϡ�����У�MnO4����H2O2Ҳ�ܷ���������ԭ��Ӧ
������Ӧ��H2O2��2e �� 2H+ + O2��
��ԭ��Ӧ��MnO4�� + 5e + 8H+ �� Mn2+ + 4H2O
��3����Ӧ������0.5 mol H2O2�μӴ˷�Ӧ��ת�Ƶ��ӵĸ���Ϊ ����������Ӧ�ó�������������ǿ���Ľ����� >___________(��д��ѧʽ)��
��4����֪��2KMnO4+ 7H2O2+3H2SO4�� K2SO4+2MnSO4 +6O2��+10H2O����1mol KMnO4������H2O2��
mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ����Լ�ȼ�ϵĿ�������������Ҫ���塣
��1��NO2����ˮ���գ����÷�Ӧ6NO2+8NH3 7N2+12H2O��
7N2+12H2O��
Ҳ���Դ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������______________L��
��2����֪��2SO2(g)+ O2 (g)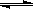 2SO3 (g)������H =��196.6kJ��mol��1
2SO3 (g)������H =��196.6kJ��mol��1
2NO(g)+ O2 (g) 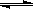 2NO2 (g)������H =��113.0kJ��mol��1
2NO2 (g)������H =��113.0kJ��mol��1
��ӦNO2(g)+ SO2 (g) 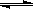 SO3 (g) +NO(g)�ġ�H =______kJ��mol��1
SO3 (g) +NO(g)�ġ�H =______kJ��mol��1
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)+ 2H2 (g) 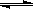 CH3OH (g)���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��1���³��һ�Ρ��ٶ��ŵ�����У��״���ȫ����������CO2�������������CO32��
CH3OH (g)���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��1���³��һ�Ρ��ٶ��ŵ�����У��״���ȫ����������CO2�������������CO32��
�ٸõ�ط�Ӧ�������ӷ���ʽΪ____________________________________________��
�ڼ״���____��������Ӧ��������������ڷŵ��������Һ��pH��____________����ͻ����������䣩������16�˼״���������ȫ����,�����ĵ��ܵ��������CuSO4��Һ����������������������������Ϊ80������������״���µ�O2________________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��16�֣������ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr(OH)3������ȥ�����ֽ����������ɳ�����pH���ұ���
| | ��ʼ������pH | ��ȫ������pH |
| Fe(OH)2 | 7.0 | 9.0 |
| Fe(OH)3 | 1.9 | 3.2 |
| Cr(OH)3 | 6.0 | 8.0 |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��6�֣���50mL a mol��L-1��������Һ�У�����6.4g Cu��ȫ���ܽ⣬��������Ļ�ԭ����ֻ��NO2��NO������Ӧ����Һ������ˮϡ����100mLʱ���c(NO3-)="3" mol��L-1��
��1����ϡ�ͺ����Һ��pH= ��
��2����a=9�������ɵ�������NO2�����ʵ���Ϊ mol��
��3����������������Ⱦ�ķ���֮һ����NaOH��Һ�������գ���Ӧԭ�����£�
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
����������NO2��NO�Ļ������ͨ��1mol��L-1��NaOHǡ�ñ����գ���NaOH��Һ�����Ϊ mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ij�о�С��Ϊ̽��SO2��Fe(NO3)3��Һ�ķ�Ӧ��ʵ�顣���������ͼ��ʾװ�ý���ʵ��.��֪��1.0 mol/L��Fe(NO3)3��Һ��pH��1
��ش�
��1��װ��A����������Ũ�������������Ϊ ��
��2��ʵ��ǰ����N2��Ŀ���� ��
��3��װ��B�в����˰�ɫ��������ɷ���_______��˵��SO2����____�ԡ�
��4������B�в�����ɫ������ԭ��
�۵�1��SO2��Fe3����Ӧ��
�۵�2��������������SO2��NO3-��Ӧ��
�����۵�1��ȷ�������������⣬��Ӧ�۲쵽�������� ��
�ڰ��۵�2��װ��B�з�Ӧ�����ӷ���ʽ�� ��
��������Ϊ���罫װ��B�е�Fe(NO3)3��Һ�滻Ϊ�������������Һ������ͬ�����½���ʵ�飬Ҳ����֤�۵�2�Ƿ���ȷ����ʱӦѡ�������Լ��ǣ�����ţ� ��
| A��1 mol/Lϡ���� |
| B��1.5 mol/L Fe(NO3)2��Һ |
| C��6.0 mol/L NaNO3��Һ��0.2 mol/L����������ϵ���Һ |
| D��3.0 mol/L NaNO3��Һ��0.1mol/L����������ϵ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ijУ��ѧʵ����ȤС���ڡ�̽��±�ص��ʵ������ԡ���ϵ��ʵ���з��֣���������ϡ�Ȼ�������Һ�У�����1��2����ˮ������Һ�ʻ�ɫ��
(1)������⣺Fe3����Br2˭�������Ը�ǿ��
(2)������룺
�ټ�ͬѧ��Ϊ�����ԣ�Fe3��>Br2��������ʵ�������Ƿ�����ѧ��Ӧ���£�����Һ�ʻ�ɫ����Ϊ���� (�ѧʽ����ͬ)��
����ͬѧ��Ϊ�����ԣ�Br2>Fe3����������ʵ�������Ƿ�����ѧ��Ӧ���£�����Һ�ʻ�ɫ����Ϊ���� ��
(3)���ʵ�鲢��֤����ͬѧΪ��֤��ͬѧ�Ĺ۵㣬ѡ������ijЩ�Լ���Ƴ����ַ�������ʵ�飬��ͨ���۲�ʵ������֤������ͬѧ�Ĺ۵�����ȷ�ġ�
��ѡ�õ��Լ���
a.��̪��Һ b�����Ȼ�̼ c����ˮ�ƾ� d�����軯����Һ
���������б�����д����ͬѧѡ�õ��Լ���ʵ���й۲쵽������(�Լ������)��
| | ѡ���Լ� | ʵ������ |
| ����1 | | |
| ����2 | | |
 ��Br����������Br2����ԭFeBr2��Һ��FeBr2�����ʵ���Ũ��Ϊ ��
��Br����������Br2����ԭFeBr2��Һ��FeBr2�����ʵ���Ũ��Ϊ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ˮ���ۺ����ÿ����Ʊ������ƺ�þ�ȣ�����������ͼ��ʾ��
����˵������ȷ���� �� ��
| A����ˮ���ζ����������仯 |
| B������ĸҺ�ɽ�һ����ȡ�壬��Ҫ���� |
| C����������������Mg(OH)2���������ӷ���ʽΪ��Mg2++Ca(OH)2= Mg(OH)2+Ca2+ |
| D�����õ��MgO����ȡþ����ΪMgO�۵�ߣ��ܺĴ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com