
 2Z(g)����H < 0�����ı�ijһ�������ﵽ��ƽ�������������ȷ����
2Z(g)����H < 0�����ı�ijһ�������ﵽ��ƽ�������������ȷ����| A����С���������Z��Ũ�Ȳ��� |
| B�������¶ȣ�X��ת�������� |
| C����������������䣬����һ�����ĺ�����Y��Ũ�Ȳ��� |
| D������ѹǿ���䣬�ٳ���0.2 mol X��0.2 mol Y��X������������� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
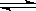 2SO3 (g)����H=��a kJ��mol��1����ͬ�����£�Ҫ��õ�2a kJ��������������ʵ����ʵ���������
2SO3 (g)����H=��a kJ��mol��1����ͬ�����£�Ҫ��õ�2a kJ��������������ʵ����ʵ���������| A��4molSO2��2molO2 | B��5molSO2��3molO2 |
| C��4molSO2��4molO2 | D��2molSO2��1molO2��2molSO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3 �SH= ��92��4 kJ/mol ��һ���¶Ⱥ����������ܱ������н��в��ﵽƽ�⣬������c (N2 )= 2mol/L��c (H2)=5mol/L����Ӧ�ﵽƽ��ʱ��һ���N2�����˷�Ӧ����
2NH3 �SH= ��92��4 kJ/mol ��һ���¶Ⱥ����������ܱ������н��в��ﵽƽ�⣬������c (N2 )= 2mol/L��c (H2)=5mol/L����Ӧ�ﵽƽ��ʱ��һ���N2�����˷�Ӧ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Y��g����Z��s����
Y��g����Z��s����| A��ѹǿ�ı仯������ͨ���ı����������ʵ�֣��Ը�ƽ��û��Ӱ�� |
| B��������ӦΪ���ȷ�Ӧ����Xһ��Ϊ��̬ |
| C����XΪ����̬��������ӦΪ���ȷ�Ӧ |
| D����XΪ��̬�����������г���a mol X���ﵽ��ƽ������һ��ƽ����ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

 2AB3��g����ѧƽ��״̬��Ӱ��ʱ���õ�����ͼ��ʾ�ı仯���ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�����������ͼʾ�ó��Ľ�����ȷ���� ��������
2AB3��g����ѧƽ��״̬��Ӱ��ʱ���õ�����ͼ��ʾ�ı仯���ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�����������ͼʾ�ó��Ľ�����ȷ���� ��������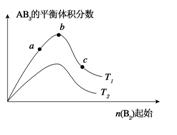
| A����Ӧ����a>b>c |
| B���ﵽƽ��ʱ��A2��ת���ʴ�СΪ��b>a>c |
| C����T2>T1��������Ӧ�����ȷ�Ӧ |
| D���ﵽƽ��ʱ��AB3�����ʵ�����СΪ��c>b>a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
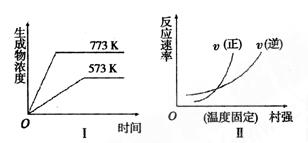
A��N2��g��+3H2(g)  2NH3(g)��H��0 2NH3(g)��H��0 |
B��2SO3��g�� 2SO2(g)+O2(g)��H��0 2SO2(g)+O2(g)��H��0 |
C��4NH3��g��+5O2(g)  4NO(g)+6H2O(g)��H��0 4NO(g)+6H2O(g)��H��0 |
D��H2(g)+CO(g)  C(s)+H2O(g)��H��0 C(s)+H2O(g)��H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����FeCl3��Һ���ɺ��ܵõ�FeCl3���� |
B�����淴Ӧ2SO2+O2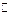 2SO3�У���SO2��O2��SO3�������ʵ���֮��Ϊ2��1��2ʱ��ʾ�Ѵ�ƽ��״̬�ı�־ 2SO3�У���SO2��O2��SO3�������ʵ���֮��Ϊ2��1��2ʱ��ʾ�Ѵ�ƽ��״̬�ı�־ |
| C����������þ�ۼӵ�NH4Cl��Һ����̬����ֻ��H2 |
| D��������ۻ�ʱ���ܵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2��g������2��g�����ﵽƽ��ʱ���n��H2��Ϊ0.5mol������˵������ȷ���� �� ��
CO2��g������2��g�����ﵽƽ��ʱ���n��H2��Ϊ0.5mol������˵������ȷ���� �� ��| A���ڸ��¶���ƽ�ⳣ��K="1" | B��ƽ�ⳣ���뷴Ӧ�¶��� |
| C��CO��ת����Ϊ50% | D��������������ʱ���ı�ѹǿƽ�ⲻ�ƶ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com