
在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通(如图9-14)。容器中发生以下反应:N2+3H2![]() 2NH3;ΔH<0。若反应达平衡后,测得混合气体为7体积。据此完成下列问题:?
2NH3;ΔH<0。若反应达平衡后,测得混合气体为7体积。据此完成下列问题:?

图9-14
(1)保持上述反应温度不变,设a、b、c分别代表起始加入的N2、H2和NH3的体积。如果反应达平衡后混合气体中各物质的百分含量仍与上述平衡时完全相同,那么:?
①若a=1、c=2,则b= 。在此情况下,反应起始时将向 (填“正”或“逆”)方向进行。?
②若需规定起始时反应向逆方向进行,则c的范围是? ?。?
(2)在上述装置中,若需控制平衡后,混合气体为6.5体积,则可采取的措施是 ,其原因是 。?
(1)①3 逆 ②1<c≤4?
(2)降低温度 反应向放热(正)反应方向进行,气体体积缩小?
解析:(1)①在同温、同压下,当起始时N2为1体积,NH3为2体积时,为保持与原平衡状态完全相同,可将2体积NH3当作完全分解成1体积N2和3体积H2。因为原来已有1体积N2,此时共有2体积N2。为使H2达到6体积,原来应有3体积H2。即b=3。由于现在平衡与原平衡全等,对比原平衡的平衡C的量可知:当a=1,b=3、c=2时,起始时v(逆)>v(正),反应向逆反应方向进行。??
②若规定起始时反应向逆方向进行,可将2体积N2和6体积H2当作完全化合成4体积NH3,即只有4体积NH3时,起始时只有逆反应发生且反应速率最快;若2体积N2和6体积H2反应生成NH3的反应已达到平衡,在此过程中,v(逆)由最小逐渐增大到与v(正)相等。要使起始时反应向逆反应方向进行,c![]() (NH3)必大于c
(NH3)必大于c![]() (NH3)。设消耗N2为x体积,则:?
(NH3)。设消耗N2为x体积,则:?
N2 + 3H2![]() 2NH3?
2NH3?
起始 2 6 0?
平衡 2-x 6-3x 2x?
依题意:(2-x)+(6-3x)+2x=7,解得:x=0.5,即c![]() (NH3)=2×0.5=1?
(NH3)=2×0.5=1?
可知c的范围是1~4之间。?
(2)原平衡时混合气体为7体积,现要减小为6.5体积,即要使反应向正(放热)方向进行,为此可在压强一定时降低反应的温度。


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
 (2011?泰州二模)能源、材料和信息是现代社会的三大“支柱”.
(2011?泰州二模)能源、材料和信息是现代社会的三大“支柱”.

查看答案和解析>>
科目:高中化学 来源: 题型:
 (2012?唐山二模)【化学--选修物质结构与性质】
(2012?唐山二模)【化学--选修物质结构与性质】



查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。
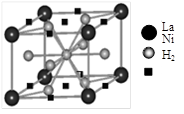
① Ni原子的价电子排布式是 ▲ 。
② 该合金储氢后,含1mol La的合金可吸附H2的数目为 ▲ 。
(2)南师大结构化学实验室合成了一种多功能材料——对硝基苯酚水合物(化学式为C6H5NO3·1.5H2O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是 ▲ 。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是 ▲ 。
(3)科学家把NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构。该阴离子的电子式是 ▲ ,其中心原子N的杂化方式是 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2012届江苏省盐城中学高三上学期期中考试化学试卷 题型:填空题
A 能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。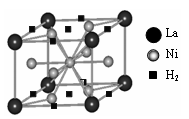
① Ni原子的价电子排布式是__________。
② 该合金储氢后,含1mol La的合金可吸附H2的
物质的量为____________________。
(2)南师大结构化学实验室合成了一种多功能材料——对硝基苯酚水合物(化学式为C6H5NO3·1.5H2O)。实验表明,加热至94℃时该晶体能失去结晶 水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是____________________。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是__________。
(3)科学家把NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8 电子稳定结构。
电子稳定结构。
该阴离子的电子式是__________,其中心原子N的杂化方式是__________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省高三上学期练习化学试卷 题型:填空题
(12分)能源、材料和信息是现代社会的三大“支柱”。
(1)目前,利用金属或合金储氢的研究已取得很大进展,下图是一种镍基合金储氢后的晶胞结构图。
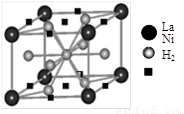
① Ni原子的价电子排布式是 ▲ 。
② 该合金储氢后,含1mol La的合金可吸附H2的数目为 ▲ 。
(2)南师大结构化学实验室合成了一种多功能材料——对硝基苯酚水合物(化学式为C6H5NO3·1.5H2O)。实验表明,加热至94℃时该晶体能失去结晶水,由黄色变成鲜亮的红色,在空气中温度降低又变为黄色,具有可逆热色性;同时实验还表明它具有使激光倍频的二阶非线性光学性质。
①晶体中四种基本元素的电负性由大到小的顺序是 ▲ 。
②对硝基苯酚水合物失去结晶水的过程中,破坏的微粒间作用力是 ▲ 。
(3)科学家把NaNO3和Na2O在一定条件下反应得到一种白色晶体,已知其中阴离子与SO42-互为等电子体,且该阴离子中的各原子的最外层电子都满足8电子稳定结构。该阴离子的电子式是 ▲ ,其中心原子N的杂化方式是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com