
·ÖĪö £Ø1£©1mL pH=1µÄH2SO4ČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½100mL£¬c£ØH+£©ÓÉ0.1mol/L±äĪŖ0.001mol/L£¬½įŗĻKw¼ĘĖćc£ØOH-£©£¬½ų¶ų¼ĘĖ涞Õß±ČÖµ£»
£Ø2£©³£ĪĀĻĀ£¬0.01mol•L-1µÄNaOHČÜŅŗµÄpHĪŖ12£¬¶ųijĪĀ¶ČŹ±²āµĆ0.01mol•L-1µÄNaOHČÜŅŗµÄpHĪŖ11£¬ŌņKWŌö“ó£»
£Ø3£©½«pH=aµÄNaOHČÜŅŗVa LÓėpH=bµÄĮņĖįVb L»ģŗĻ£¬ČōĖłµĆ»ģŗĻČÜŅŗµÄpH=10£¬¼ī¹żĮ棬¼ĘĖć³öc£ØOH-£©ÓėĖį¼īµÄĪļÖŹµÄĮæµÄ¹ŲĻµ£¬æɼĘĖć£»
½ā“š ½ā£ŗ1mL pH=1µÄH2SO4ČÜŅŗ¼ÓĖ®Ļ”ŹĶµ½100mL£¬c£ØH+£©ÓÉ0.1mol/L±äĪŖ0.001mol/L£¬c£ØOH-£©=$\frac{1{0}^{-14}}{1{0}^{-3}}$mol/L=10-11mol/L£¬Ōņ$\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$=108£¬
¹Ź“š°øĪŖ£ŗ108£»
£Ø2£©³£ĪĀĻĀ£¬0.01mol•L-1µÄNaOHČÜŅŗµÄpHĪŖ12£¬¶ųijĪĀ¶ČŹ±²āµĆ0.01mol•L-1µÄNaOHČÜŅŗµÄpHĪŖ11£¬ŌņKW=0.01”Į10-11=1.0”Į10-13£¬ĪĀ¶ČøßÓŚ25”ę£¬
¹Ź“š°øĪŖ£ŗ1.0”Į10-13£»£¾£»
£Ø3£©½«pH=aµÄNaOHČÜŅŗVa LÓėpH=bµÄĮņĖįVb L»ģŗĻ£¬ČōĖłµĆ»ģŗĻČÜŅŗµÄpH=10£¬¼ī¹żĮ棬c£ØOH-£©=$\frac{0.1{V}_{a}-0.01{V}_{b}}{{V}_{a}+{V}_{b}}$=0.001£¬ŌņVa£ŗVb=1£ŗ9£¬
¹Ź“š°øĪŖ£ŗ1£ŗ9£®
µćĘĄ ±¾Ģāæ¼²épHµÄ¼ĘĖć£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦µÄ漲飬Ć÷Č·ÅضČÓėpHµÄ»»ĖćŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | FeCl2 | B£® | FeCl3 | C£® | Na2S | D£® | Fe3O4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2æÉÓĆÓŚĘÆ°×Ö½½¬ | B£® | SiO2ŹĒĮ¼ŗƵİėµ¼Ģå²ÄĮĻ | ||
| C£® | Na2O2æÉÓĆ×÷Ē±Ė®Ķ§O2Ą“Ō“ | D£® | Cl2æÉÓĆÓŚĻū¶¾ŗĶÖĘŌģĘÆ°×·Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ū¢Ż¢ß¢ą | B£® | ¢Ł¢Ü¢Ž¢ß | C£® | ¢Ł¢Ś¢Ū¢ß¢ą | D£® | ¢Ś¢Ū¢Ż¢Ž¢ß¢ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
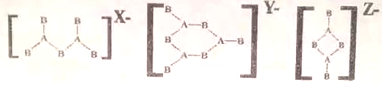
| A£® | 4”¢4”¢2 | B£® | 4”¢3”¢2 | C£® | 3”¢3”¢2 | D£® | 4”¢2”¢2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2CO3+H2SO4ØTCO2”ü+H2O+Na2SO4 | B£® | CO2+2NaOHØTNa2CO3+H2O | ||
| C£® | CO2+2Mg$\frac{\underline{\;µćČ¼\;}}{\;}$ 2MgO+C | D£® | CO2+Na2O=Na2CO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ²»ČÜĪļŅ»¶ØŹĒĶ | |
| B£® | ²»ČÜĪļŅ»¶ØŹĒĢś | |
| C£® | ²»ČÜĪļÖŠŅ»¶Øŗ¬Ķ£¬µ«²»Ņ»¶Øŗ¬Ģś | |
| D£® | ĀĖŅŗÖŠŅ»¶Øŗ¬ÓŠFeSO4£¬Ņ»¶ØƻӊCuSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±äŠ” | B£® | ±ä“ó | C£® | ²»±ä | D£® | ĪŽ·ØČ·¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com