
| A. | 4L | B. | 6L | C. | 8L | D. | 12L |
分析 NO2和NO的混合气体通入水后发生反应为3NO2+H2O=2HNO3+NO,导致气体体积减小,计算出体积变化量,根据体积差量法计算NO2的体积,再根据二氧化氮与水的反应方程式判断被氧化的二氧化氮的体积.
解答 解:反应后体积减小为15L-7L=8L,则:
3NO2+H2O=2HNO3+NO 体积减小△V
3 2
V(NO2) 8L
解得:V(NO2)=$\frac{8L×3}{2}$=12L,
根据反应3NO2+H2O=2HNO3+NO可知,二氧化氮被氧化生成硝酸,参加反应的二氧化氮中被氧化的占参加反应的二氧化氮$\frac{2}{3}$,
则被氧化的二氧化氮的体积为:12L×$\frac{2}{3}$=8L,
故选C.
点评 本题考查了混合物反应的计算,题目难度中等,明确反应原理及差量法的应用为解答关键,注意掌握氧化还原反应中反应类型的判断方法,试题培养了学生灵活应用基础知识的能力.


科目:高中化学 来源: 题型:选择题
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| B. | 用铜板做电极电解硫酸铜溶液,阴极铜板质量增加 | |
| C. | 把铜片插入氯化铁溶液中,加入几滴氯化铜溶液,气泡放出的速率加大 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出的速率加大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | 碳棒 | C. | MnO2 | D. | MnO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
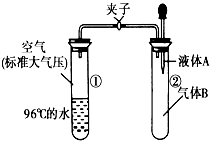 如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的( )
如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了,则液体A和气体B的组合不可能是下列的( )| A. | 氢氧化钠溶液、二氧化碳 | B. | 水、氨气 | ||
| C. | 氢氧化钠溶液、一氧化氮 | D. | 水、二氧化氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠原子失去一个电子后,它的电子数与氖原子相同,所以变成氖原子 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子组成的 | |
| C. | 核素指一种原子,而元素是指一类原子;核素间互称同位素,元素包含同位素 | |
| D. | ${\;}_{18}^{40}$Ar、${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca的质量数相同,所以它们是互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液(Na2CO3),应通入过量的CO2气体 | |
| B. | NaBr溶液(NaI),应加入适量的氯水、CCl4,进行萃取分液 | |
| C. | NH4Cl溶液(FeCl3),应加入适量的氨水,过滤 | |
| D. | CO2(CO),通过过量的灼热的氧化铜粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )| A. | 1mo N2(g)和1mo O2(g)完全反应放出的能量为180kJ | |
| B. | 通常情况下,N2(g)和O2(g)混合能直接生成NO | |
| C. | 1mol N2(g)和1molO2(g)具有的总能量小于2molN(g)具有的总能量 | |
| D. | NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操作 | 现象 |
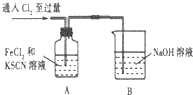 | 1.A中溶液变红 2.稍后,A中溶液由红色变为黄色 |
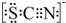 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com