
在允许加热的条件下,只用一种试剂就可以鉴别(NH4)2SO4、KCl、MgCl2、Al2(SO4)3和Fe2(SO4)3溶液,这种试剂是 ( )
A.NaOH B.NH3·H2O
C.AgNO3 D.BaCl2
A
【解析】
试题分析:A、NaOH与(NH4)2SO4加热反应有刺激性气味气体产生;与KCl不反应,无明显现象;与MgCl2反应生成白色沉淀;与Al2(SO4)3反应生成白色沉淀,当NaOH过量时,白色沉淀溶解;与Fe2(SO4)3反应时,有红褐色沉淀产生,现象不同,能鉴别,故A正确;B、一水合氨与(NH4)2SO4、KCl均不反应,与MgCl2、Al2(SO4)3均生成白色沉淀,现象相同,不能鉴别,故B错误;C、AgNO3与以上几种物质反应,均生成白色沉淀,现象相同,不能鉴别,故C错误;D、BaCl2与(NH4)2SO4、Al2(SO4)3和Fe2(SO4)3溶液均生成白色沉淀,现象相同,不能鉴别,故D错误。
考点:本题考查物质的鉴别。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届安徽省黄山市高三第一次月考化学试卷(解析版) 题型:选择题
下列除去杂质的方法不正确的是 ( )
A.除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体
B.除去Na2CO3固体中少量NaHCO3:置于坩埚中加热
C.除去苯中溶有的少量苯酚: 加入适量浓溴水反应后过滤
D.除去FeCl3酸性溶液中少量的FeCl2:通入稍过量的Cl2
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高一上学期期中考试化学试卷(解析版) 题型:选择题
下表中评价合理的是
选项 | 化学反应及其离子方程式 | 评价 |
A. | NaHSO4溶液与Ba(OH)2溶液反应至中性: 2H++SO42﹣+Ba2++2OH﹣=BaSO4↓+2H2O | 正确 |
B. | 向碳酸镁中加入足量稀盐酸: MgCO3+2H+=Mg2++CO2↑+H2O | 错误,碳酸镁应拆成离子形式 |
C. | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色: Fe3++3H2O=Fe(OH)3↓+3H+ | 正确 |
D. | NaOH溶液中通入少量CO2反应:OH﹣+CO2=HCO3﹣ | 正确 |
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各组选项按电解质、非电解质、单质和混合物顺序排列的一组是
A.HCl、SO3、石墨、液氧
B.蔗糖、CuSO4、氮气、波尔多液
C.NaCl、乙醇、铁、空气
D.KCl、NaNO3、氯气、石灰水
查看答案和解析>>
科目:高中化学 来源:2015届安徽省铜陵市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列关于溶液和胶体的叙述中,正确的是( )
A. 胶体带电荷,而溶液呈电中性
B.胶体加入电解质溶液可产生沉淀,而溶液不能
C.胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系
D.胶体和溶液都能产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源:2015届安徽省铜陵市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列实验能达到目的的是 ( )
A.在容量瓶中加一定体积的水,再加入浓盐酸配制准确浓度的稀盐酸
B.用稀硫酸和锌粒反应制氢气时加入少许硫酸铜加快反应速率
C.用玻璃棒搅拌漏斗中的液体以加快过滤的速度
D.加入盐酸以除去硫酸钠中的少量碳酸钠杂质
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三第一次联考化学试卷(解析版) 题型:填空题
(1)在常温下,0.5mol甲醇在氧气中完全燃烧生成CO2和液态水,放出热量363.3kJ.写出该反应的热化学方程式: _________________________
(2)请设计一个燃料电池:电解质为强碱溶液,Pt作电极,在电极上分别通入甲醇和氧气。通入甲醇的电极应为 极(填“正”或“负”),该电极上发生的电极反应式为 。
(3)用Pt电极电解盛有1L pH=6的硝酸银溶液,如图甲所示,则右边电极上发生的电极反应式为 .
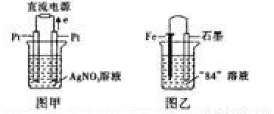
(4)某化学学习兴趣小组为了研究金属的腐蚀现象,将一枚铁钉放在“84”消毒液(NaClO)中,某同学设计了如图乙所示实验装置,写出石墨极上发生的电极反应式:
查看答案和解析>>
科目:高中化学 来源:2015届安徽省皖南八校高三第一次联考化学试卷(解析版) 题型:实验题
(12分)某研究小组为了探究Fe3+与I-的反应是否为可逆反应,设计了如下实验:
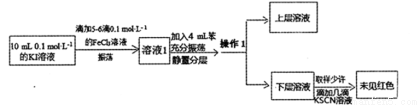
(1)取少量溶液1于试管中,加入少量淀粉溶液,震荡,溶液变蓝,说明Fe3+与I-的反应有______________生成(填化学式)。
(2)上述操作1的名称:______________,所用的主要仪器是_____________,上层溶液的颜色为________________。
(3)该小组对下层溶液滴加KSCN溶液未见红色的原因,提出了下列两种猜想。
猜想一:___________________________;
猜想二:残留的Fe3+与SCN-结合生成的Fe(SCN)3浓度极小,其溶液颜色肉眼无法观察。
为了验证猜想,在查阅资料后,获得下列信息:
Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高。
(4)若猜想1成立,请写出该反应的离子方程式:______________;
(5)若猜想2成立,请自行设计实验验证。
实验步骤 | 预期现象与结论 |
|
|
查看答案和解析>>
科目:高中化学 来源:2015届宁夏银川市高三上学期期中考试化学试卷(解析版) 题型:填空题
研究性学习小组用Na2SO3与硫酸溶液(硫酸与水体积比1∶1)制备SO2并进行性质探究实验。
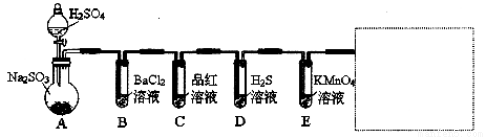
D中的实验现象是 ,C、E中溶液都褪色,分别体现SO2 、 性质。
(2)需在方框中画出 装置, 装置(只填写,不画图)。
(3)研究小组发现B中有白色沉淀,为了清楚沉淀的物质,研究小组往B中加入过量稀盐酸,沉淀不溶解,你认为留下的沉淀物是 ,形成该沉淀的反应方程式有: 。
为了进一步验证沉淀原因,研究小组另取BaC12溶液,加热煮沸,冷却及时加入少量苯液封,然后再通SO2,结果发现沉淀量减少,但仍有轻微浑浊。研究小组改进A装置(如图),再进行实验,B中没有出现浑浊。下列气体可作为X气体的是 (填序号,不定项选择)
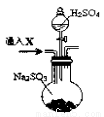
A.CO2 B.NH3 C.O3 D.N2 E.NO2
SO2为空气污染物,研究小组为测定某工厂区空气中SO2的含量,取10m3(标准状况)的空气,缓慢通过足量溴水中,在所得溶液中加入过量的BaC12溶液,将产生的白色沉淀洗涤、干燥,用电子称称其质量为0.233g,则:①沉淀洗涤要干净,检验洗涤已经干净的实验操作是 。
②试计算此空气中SO2的浓度(列出计算表达式并计算结果,结果单位用mg/m3表示) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com