
ĄūĖâÄŋĄŋÂĖËŪĮāÉ―ūÍĘĮ―ðÉ―ãyÉ―ĢŽÉúēúÉúŧîÖÐÎÛČūÎïĩÄšÏĀíīĶĀíķÔŧ·ūģąĢŧĪūßÓÐÖØŌŠŌâŌåĄĢ
(1)ĀûÓÃÄģÐĐīßŧŊžÁĢŽģÉđĶĘĩÏÖ―ŦŋÕÆøÖÐĩÄĖžŅõŧŊšÏÎïšÍĩŠŅõŧŊšÏÎïŨŠŧŊΊÎÞķūĩÄīóÆøŅŧ·ÎïÖĘĄĢ
ŌŅÖŠĢšĒŲ![]()
![]()
ĒÚNO(g)+CO(g)![]()
![]() N2(g)+CO2(g)
N2(g)+CO2(g)![]()
ĒÛ2NO(g)+O2(g)![]() 2NO2(g)
2NO2(g) ![]()
·īÓĶ![]() ĩÄ
ĩÄ![]() ________
________![]() ĢŧÄģÎÂķČÏÂĢŽ·īÓĶĒŲĒÚĒÛĩÄÆ―šâģĢĘý·ÖeĨŦ
ĢŧÄģÎÂķČÏÂĢŽ·īÓĶĒŲĒÚĒÛĩÄÆ―šâģĢĘý·ÖeĨŦ![]() ĄĒ
ĄĒ![]() ĄĒ
ĄĒ![]() ĢŽÔōļ÷īÓĶĩÄK=________(ÓÃ
ĢŽÔōļ÷īÓĶĩÄK=________(ÓÃ![]() ĄĒ
ĄĒ![]() ĄĒ
ĄĒ![]() ąíĘū)ĄĢ
ąíĘū)ĄĢ
(2)ÎÂķČΊ![]() Ąæ
žĢŽÔÚËÄļöČÝŧýūųΊ1LĩÄšãČÝÃÜąÕČÝÆũÖзĒÉú·īÓĶĢš
Ąæ
žĢŽÔÚËÄļöČÝŧýūųΊ1LĩÄšãČÝÃÜąÕČÝÆũÖзĒÉú·īÓĶĢš
![]()
![]() ĢŽēâĩÃÓÐđØĘĩŅéĘýūÝČįÏÂĢš
ĢŽēâĩÃÓÐđØĘĩŅéĘýūÝČįÏÂĢš
ČÝÆũąāšÅ | ÎïÖĘĩÄÆðĘžÅĻķČ( | ÎïÖĘĩÄÆ―šâÅĻķČ( | |
|
|
| |
Ēņ |
|
|
|
Ēō |
|
| |
Ēó |
|
| |
Ēô |
|
| |
ĒŲÆ―šâĘąĢŽČÝÆũĒōÓëĒôČÝÆũĩÄŨÜŅđĮŋÖŪąČ___________ĄĢ
ĒÚÎÂķČēŧąäĢŽČÝÆũĒóÖÐīïĩ―Æ―šâšóÔŲģäČëNOĄĒ![]() (g)ļũ
(g)ļũ![]() molĢŽÔō·īÓĶ―ŦÏō_____________ĄĢ(ĖÕýĄąŧōĄ°ÄæĄą)·―Ïō―øÐÐĄĢ
molĢŽÔō·īÓĶ―ŦÏō_____________ĄĢ(ĖÕýĄąŧōĄ°ÄæĄą)·―Ïō―øÐÐĄĢ
(3)ģĢÎÂÏÂÓÃ0.100![]() ŅÎËá·ÖąðĩÎķĻ10.00mLÅĻķČūųΊ0.100
ŅÎËá·ÖąðĩÎķĻ10.00mLÅĻķČūųΊ0.100![]() ĩÄNaOHČÜŌššÍķþžŨ°·[
ĩÄNaOHČÜŌššÍķþžŨ°·[![]() ]ČÜŌš(ÔÚËŪÖÐĩįĀë·―Ę―Óë°ąÏāËÆ)ĢŽĀûĩįÓÃīŦļÐÆũēâĩÃĩÎķĻđýģĖÖÐČÜŌšĩÄĩįĩžÂĘČįÍžËųĘūĄĢŌŅÖŠĩį―âÖĘČÜŌšĩįĩžÂĘÔ―īóĩžĩįÄÜÁĶÔ―ĮŋĄĢ
]ČÜŌš(ÔÚËŪÖÐĩįĀë·―Ę―Óë°ąÏāËÆ)ĢŽĀûĩįÓÃīŦļÐÆũēâĩÃĩÎķĻđýģĖÖÐČÜŌšĩÄĩįĩžÂĘČįÍžËųĘūĄĢŌŅÖŠĩį―âÖĘČÜŌšĩįĩžÂĘÔ―īóĩžĩįÄÜÁĶÔ―ĮŋĄĢ
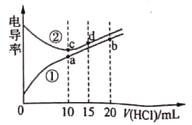
ĒŲaĄĒbĄĒcĄĒdËÄĩãĩÄËŪČÜŌšÖÐĢŽÓÉËŪĩįĀëģöĮâĀëŨÓÅĻķČīóÓÚ![]()
![]() ĩÄĘĮ________________ĢŽÔŌōΊ_____________________ĄĢ
ĩÄĘĮ________________ĢŽÔŌōΊ_____________________ĄĢ
ĒÚŧŊŅ§·īÓĶÍųÍų°éÓÐČČЧÓĶČôΊūøČČĖåÏĩaĩÄÎÂķČ______________(Ė>ĄąĢŽĄ°=ĄąŧōĄ°<Ąą)cĩãĩÄÎÂķČĄĢ
Ąūīð°ļĄŋ-234.0 K2![]() 1Ģš1 Äæ a īËĘąĮĄšÃÉúģÉĮŋËáČõžîŅÎĢŽķÔËŪĩÄĩįĀëÓÐīŲ―øŨũÓà <
1Ģš1 Äæ a īËĘąĮĄšÃÉúģÉĮŋËáČõžîŅÎĢŽķÔËŪĩÄĩįĀëÓÐīŲ―øŨũÓà <
Ąū―âÎöĄŋ
ĢĻ1ĢĐļųūÝļĮËđķĻÂÉ―øÐОÆËãĢŧ
ĢĻ2ĢĐĀûÓÃČýķÎĘ―ĢŽļųūÝÆ―šâģĢĘýÖŧÓëÎÂķČÓÐđØĢŽÎÂķČēŧąäĢŽÆ―šâģĢĘýēŧąäĢŽ―ášÏĘýūÝ―øÐÐĮóËãĢŧ
(3) ĒŲNaOHĘôÓÚĮŋžîĢŽķþžŨ°·ĩÄËŪČÜŌšĘôÓÚČõžîČÜŌšĢŽĮúÏßĒŲΊĩÎķĻķþžŨ°·ČÜŌšĢŧĮŋËáČõžîŅÎĢŽķÔËŪĩÄĩįĀëÓÐīŲ―øŨũÓÃĢŧ
ĒÚËážîÖКͷīÓĶΊ·ÅČČ·īÓĶĢŽķþžŨ°·ĩÄĩįĀëÎüČČĢŽČôΊūøČČĖåÏĩaĩÄÎÂķČ<cĩãĩÄÎÂķČĄĢ
ĢĻ1ĢĐŌŅÖŠĢšĒŲ![]()
![]()
ĒÚ![]()
![]()
ĒÛ![]()
![]()
ļųūÝļĮËđķĻÂÉĢŽÓÉĒÚ+ĒŲĄÁ![]() -ĒÛĄÁ
-ĒÛĄÁ![]() ĩ÷īÓĶ
ĩ÷īÓĶ![]() ĩÄ
ĩÄ![]() +
+![]() ĄÁ
ĄÁ![]() -
-![]() ĄÁ
ĄÁ![]() =-234.0
=-234.0![]() ĢŧļųūÝŌÔÉÏ·īÓĶŋÉÖŠĢŽÄģÎÂķČÏÂĢŽ·īÓĶĒŲĒÚĒÛĩÄÆ―šâģĢĘý·ÖeΊ
ĢŧļųūÝŌÔÉÏ·īÓĶŋÉÖŠĢŽÄģÎÂķČÏÂĢŽ·īÓĶĒŲĒÚĒÛĩÄÆ―šâģĢĘý·ÖeΊ![]() ĄĒ
ĄĒ![]() ĄĒ
ĄĒ![]() ĢŽÔōļ÷īÓĶĩÄK=K2
ĢŽÔōļ÷īÓĶĩÄK=K2![]() Ģŧ
Ģŧ
ĢĻ2ĢĐšãΚãČÝÏÂĢŽĖåÏĩĩÄŅđĮŋąČĩČÓÚÆøĖåĩÄÎïÖĘĩÄÁŋÖŪąČĢŽķÔÓÚ·īÓĶĒōÓÐĢš
2NO(g) + 2H2(g) ![]() N2(g) + 2H2O(g)
N2(g) + 2H2O(g)
ÆðĘžĢš 6 2 0 0
·īÓĶĢš x x 0.5x x
Æ―šâĢš 6-x 2-x 0.5x x
ķÔÓÚ·īÓĶĒôÓÐĢš
2NO(g) + 2H2(g) ![]() N2(g) + 2H2O(g)
N2(g) + 2H2O(g)
ÆðĘžĢš 2 6 0 0
·īÓĶĢš y y 0.5y y
Æ―šâĢš 2-y 6-y 0.5y y ĢĻŌÔÉÏĩĨÎŧķžĘĮ10-3mol/LĢĐ
ĒŲÎÂķČÏāÍŽÁ―ļö·īÓĶĩÄÆ―šâģĢĘýąØČŧÏāĩČĢŽÁÐģöÆäÆ―šâģĢĘýžÆËãĘ―K=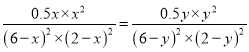 ĢŽŌŧķĻĩÃĩ―x=yĄĢÔōĩÃĩ―īïÆ―šâĘąÁ―ļö·īÓĶĖåÏĩĩÄÆøĖåŨÜÎïÖĘĩÄÁŋÏāĩČĢŽËųŌÔŅđĮŋÏāĩČĢŽđĘÆ―šâĘąĢŽČÝÆũĒōÓëĒôČÝÆũĩÄŨÜŅđĮŋÖŪąČΊ1Ģš1Ģŧ
ĢŽŌŧķĻĩÃĩ―x=yĄĢÔōĩÃĩ―īïÆ―šâĘąÁ―ļö·īÓĶĖåÏĩĩÄÆøĖåŨÜÎïÖĘĩÄÁŋÏāĩČĢŽËųŌÔŅđĮŋÏāĩČĢŽđĘÆ―šâĘąĢŽČÝÆũĒōÓëĒôČÝÆũĩÄŨÜŅđĮŋÖŪąČΊ1Ģš1Ģŧ
ĒÚķÔÓÚ·īÓĶĒņÓÐĢš
2NO(g) + 2H2(g) ![]() N2(g) + 2H2O(g)
N2(g) + 2H2O(g)
ÆðĘžĢš 0.006 0.001 0 0
·īÓĶĢš 0.0004 0.0004 0.0002 0.0004
Æ―šâĢš 0.0056 0.0006 0.0002 0.0004
K=![]() =2.83Ģŧ
=2.83Ģŧ
ČÝÆũIIIÆðĘžģäČëNOĄĒH2ĩÄÅĻķČŌĀīÎΊ1ĄÁ10-3mol/LĄĒ6ĄÁ10-3mol/LĢŽļųūÝ·―ģĖĘ―ĩÄĖØĩãĢŽÎÂķČēŧąäĢŽČÝÆũĒņÓëČÝÆũĒóĩÄÆ―šâģĢĘýÏāĩČĢŽČÝÆũIIIīïĩ―Æ―šâĘąNOĄĒH2ĄĒN2ĄĒH2OĢĻgĢĐĩÄÎïÖĘĩÄÁŋÅĻķČŌĀīÎΊ0.0006mol/LĄĒ0.0056mol/LĄĒ0.0002mol/LĄĒ0.0004mol/LĢŽËųŌÔģäČëNOĄĒH2O(gĢĐļũ2ĄÁ10-4molĢŽÔōQ=![]() =3.59>KĢŽđĘ·īÓĶ―ŦÏōÄæ·īÓĶ·―Ïō―øÐÐĢŧ
=3.59>KĢŽđĘ·īÓĶ―ŦÏōÄæ·īÓĶ·―Ïō―øÐÐĢŧ
(3) ĒŲNaOHĘôÓÚĮŋžîĢŽķþžŨ°·ĩÄËŪČÜŌšĘôÓÚČõžîČÜŌšĢŽĮúÏßĒŲΊĩÎķĻķþžŨ°·ČÜŌšĢŧžîŧōËáđýÁŋĢŽŧáŌÖÖÆËŪĩÄĩįĀëĢŽŅÎĀāËŪ―âīŲ―øËŪĩÄĩįĀëĢŽĩÎķĻÖÕĩãĮ°žîđýÁŋĢŽĩÎķĻÖÕĩãšóËáđýÁŋĢŽĮĄšÃÍęČŦĩÎķĻĘąÐÎģÉŅÎĢŽNaClēŧŧáËŪ―âĢŽķø(CH3ĢĐ2NH2+ŧáËŪ―âĢŽžÓČë10mLŅÎËáĘąĮĄšÃÍęČŦ·īÓĶĢŽŌōīËĢŽaĄĒbĄĒcĄĒdËÄĩãĩÄČÜŌšÖÐĢŽaĩãÓÉËŪĩįĀëģöĮâĀëŨÓÅĻķČīóÓÚ![]()
![]() ĢŧŌōΊīËĘąĮĄšÃÉúģÉĮŋËáČõžîŅÎĢŽķÔËŪĩÄĩįĀëÓÐīŲ―øŨũÓÃĢŧ
ĢŧŌōΊīËĘąĮĄšÃÉúģÉĮŋËáČõžîŅÎĢŽķÔËŪĩÄĩįĀëÓÐīŲ―øŨũÓÃĢŧ
ĒÚËážîÖКͷīÓĶΊ·ÅČČ·īÓĶĢŽķþžŨ°·ĩÄĩįĀëÎüČČĢŽČôΊūøČČĖåÏĩaĩÄÎÂķČ<cĩãĩÄÎÂķČĄĢ


 ĖėĖėÏōÉÏŌŧąūšÃūíÏĩÁÐīð°ļ
ĖėĖėÏōÉÏŌŧąūšÃūíÏĩÁÐīð°ļ ÐĄŅ§Éú10·ÖÖÓÓĶÓÃĖâÏĩÁÐīð°ļ
ÐĄŅ§Éú10·ÖÖÓÓĶÓÃĖâÏĩÁÐīð°ļ
| Äęžķ | ļßÖÐŋÎģĖ | Äęžķ | ģõÖÐŋÎģĖ |
| ļßŌŧ | ļßŌŧÃâ·ŅŋÎģĖÍÆžöĢĄ | ģõŌŧ | ģõŌŧÃâ·ŅŋÎģĖÍÆžöĢĄ |
| ļßķþ | ļßķþÃâ·ŅŋÎģĖÍÆžöĢĄ | ģõķþ | ģõķþÃâ·ŅŋÎģĖÍÆžöĢĄ |
| ļßČý | ļßČýÃâ·ŅŋÎģĖÍÆžöĢĄ | ģõČý | ģõČýÃâ·ŅŋÎģĖÍÆžöĢĄ |
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋÄŋĮ°ČŦĘĀ―įĩÄÄøĢĻNiĢĐÏû·ŅÁŋ―öīÎÓÚÍĄĒÂÁĄĒĮĶĄĒÐŋĢŽūÓÓÐÉŦ―ðĘôĩÚÎåÎŧĄĢÄøģĢÓÃÓÚļũÖÖļßđâÔóŨ°ĘÎÆášÍËÜÁÏÉúēúĢŽŌēģĢÓÃŨũīßŧŊžÁĄĢ
žîĘ―ĖžËáÄøĩÄÖÆąļĢš
đĪŌĩÓÃĩį―âÄøÐÂŌšĢĻÖũŌŠšŽNiSO4ĢŽNiCl2ĩČĢĐÖÆąļžîĘ―ĖžËáÄøū§Ėå[xNiCO3ĄĪyNi(OH)2ĄĪzH2O]ĢŽÖÆąļÁũģĖČįÍžĢš
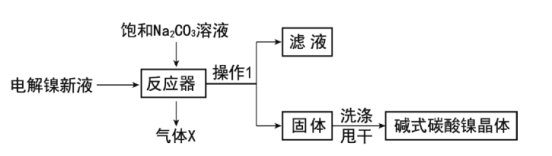
ĢĻ1ĢĐ·īÓĶÆũÖÐĩÄŌŧļöÖØŌŠ·īÓĶΊ3NiSO4+3Na2CO3+2H2O=NiCO3ĄĪ2Ni(OH)2+3Na2SO4+2XĢŽXĩÄŧŊŅ§Ę―Ί__ĄĢ
ĢĻ2ĢĐÎïÁÏÔÚ·īÓĶÆũÖзīÓĶĘąÐčŌŠŋØÖÆ·īÓĶÎÂķČšÍpHÖĩĄĢ·ÖÎöČįÍžĢŽ·īÓĶÆũÖÐŨîĘĘšÏĩÄpHÖĩΊ__ĄĢ

ĢĻ3ĢĐžėŅéžîĘ―ĖžËáÄøū§ĖåÏīĩÓļÉūŧĩÄ·―·ĻĘĮ__ĄĢ
ēâķĻžîĘ―ĖžËáÄøū§ĖåĩÄŨéģÉĢš
ΊēâķĻžîĘ―ĖžËáÄøū§Ėå[xNiCO3ĄĪyNi(OH)2ĄĪzH2O]ŨéģÉĢŽÄģÐĄŨéÉčžÆÁËČįÍžĘĩŅé·―°ļž°Ũ°ÖÃĢš

ŨĘÁÏŋĻÆŽĢšžîĘ―ĖžËáÄøū§ĖåĘÜČČŧáÍęČŦ·Ö―âÉúģÉNiOĄĒCO2šÍH2O
ĘĩŅéē―ÖčĢš
ĒŲžėēéŨ°ÖÃÆøÃÜÐÔĢŧ
ĒÚŨžČ·ģÆÁŋ3.77gžîĘ―ĖžËáÄøū§Ėå[xNiCO3ĄĪyNi(OH)2ĄĪzH2O]·ÅÔÚBŨ°ÖÃÖÐĢŽÁŽ―ÓŌĮÆũĢŧ
ĒÛīōŋŠĩŊŧÉžÐaĢŽđÄČëŌŧķÎĘąžäŋÕÆøĢŽ·ÖąðģÆÁŋŨ°ÖÃCĄĒDĄĒEĩÄÖĘÁŋēĒžĮžĢŧ
ĒÜ__Ģŧ
ĒÝīōŋŠĩŊŧÉžÐaŧšŧšđÄČëŌŧķÎĘąžäŋÕÆøĢŧ
ĒÞ·ÖąðŨžČ·ģÆÁŋŨ°ÖÃCĄĒDĄĒEĩÄÖĘÁŋēĒžĮžĢŧ
ĒßļųūÝĘýūÝ―øÐОÆËãĢĻÏāđØĘýūÝČįÏÂąíĢĐ
Ũ°ÖÃC/g | Ũ°ÖÃD/g | Ũ°ÖÃE/g | |
žÓČČĮ° | 250.00 | 190.00 | 190.00 |
žÓČČšó | 251.08 | 190.44 | 190.00 |
ĘĩŅé·ÖÎöž°ĘýūÝīĶĀíĢš
ĢĻ4ĢĐEŨ°ÖÃĩÄŨũÓÃ__ĄĢ
ĢĻ5ĢĐēđģäĒÜĩÄĘĩŅéēŲŨũ___ĄĢ
ĢĻ6ĢĐÍĻđýžÆËãĩÃĩ―žîĘ―ĖžËáÄøū§ĖåĩÄŨéģÉ__ĢĻĖîŧŊŅ§Ę―ĢĐĄĢ
ÄøĩÄÖÆąļĢš

ĢĻ7ĢĐÐīģöÖÆąļNiĩÄŧŊŅ§·―ģĖĘ―__ĄĢ
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋ°īŌŠĮóŧØīðÏÂÁÐÎĘĖâĄĢ
(1)![]() ŋÉČÜ―âÔÚ
ŋÉČÜ―âÔÚ![]() ČÜŌšÖÐĩÄÔŌōĘĮ____________________________________________________ĄĢ
ČÜŌšÖÐĩÄÔŌōĘĮ____________________________________________________ĄĢ
(2)Öą―ÓÕô·Ē![]() ČÜŌšĢŽÄÜēŧÄÜĩÃĩ―
ČÜŌšĢŽÄÜēŧÄÜĩÃĩ―![]() ū§ĖåĢŽÆäÕýČ·ĩÄēŲŨũ__________________________ĄĢ
ū§ĖåĢŽÆäÕýČ·ĩÄēŲŨũ__________________________ĄĢ
(3)ÔÚ![]() ČÜŌšÖÐĩΞӷÓĖŠĢŽČÜŌšąäšėÉŦĢŽČôÔÚļÃČÜŌšÖÐĩÎČëđýÁŋĩÄ
ČÜŌšÖÐĩΞӷÓĖŠĢŽČÜŌšąäšėÉŦĢŽČôÔÚļÃČÜŌšÖÐĩÎČëđýÁŋĩÄ![]() ČÜŌšĢŽÏÖÏóĘĮ_________________________________________________ĢŽĮë―ášÏĀëŨÓ·―ģĖĘ―ĢŽÔËÓÃÆ―šâÔĀí―øÐÐ―âĘÍĢš________________________________________________________________________ĄĢ
ČÜŌšĢŽÏÖÏóĘĮ_________________________________________________ĢŽĮë―ášÏĀëŨÓ·―ģĖĘ―ĢŽÔËÓÃÆ―šâÔĀí―øÐÐ―âĘÍĢš________________________________________________________________________ĄĢ
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
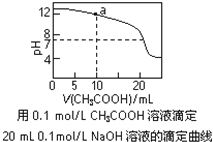
ĄūĖâÄŋĄŋÏÂÁÐÓÐđØČÜŌšÖÐÁĢŨÓÅĻķČĩÄđØÏĩĘ―ÖÐĢŽÕýČ·ĩÄĘĮ(ĄĄĄĄ)
A.pHÏāÍŽĩÄĒŲCH3COONaĄĒĒÚNaHCO3ĄĒĒÛNa2CO3Čý·ÝČÜŌšÖÐĩÄc(NaĢŦ)ĢšĒÛĢūĒÚĢūĒŲ
B.0.1molĄĪLĢ1ÄģķþÔŠČõËáĮŋžîŅÎNaHAČÜŌšÖÐĢšc(Na+)=2c(A2-)ĢŦc(HA-)ĢŦc(H2A)
C.ÍžÖÐaĩãČÜŌšÖÐļũĀëŨÓÅĻķČĩÄđØÏĩĘĮĢšc(OHĢ)Ģ―c(HĢŦ)ĢŦc(CH3COOĢ)ĢŦ2c(CH3COOH)
D.ÍžÖÐpHĢ―7ĘąĢšc(NaĢŦ)Ģūc(CH3COOĢ) Ģūc(OHĢ)Ģ―c(HĢŦ)
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋŧŊšÏÎï![]() (
( )ĘĮŌŧÖÖŌšĖŽŧŊšÏÎïĢŽ·Ðĩã77 ĄæĢŽÔÚĘĒÓÐ
)ĘĮŌŧÖÖŌšĖŽŧŊšÏÎïĢŽ·Ðĩã77 ĄæĢŽÔÚĘĒÓÐ![]() ËŪĩÄŨķÐÎÆŋÖÐÐĄÐÄĩØĩΞÓ8ĄŦ10ĩÎ
ËŪĩÄŨķÐÎÆŋÖÐÐĄÐÄĩØĩΞÓ8ĄŦ10ĩÎ![]() ĢŽŋÉđÛēėĩ―·īÓĶūįÁŌĢŽŌšÃæÉÏÓаŨÎíÐÎģÉĢŽēĒŌÝģöÓÐÆøÎķĩÄÆøĖåĢŽļÃÆøĖåŋÉĘđÕīÓÐÆ·šėĘÔŌšĩÄÂËÖ―ÍĘÉŦĄĢĮáĮáÕņĩīŨķÐÎÆŋĢŽīý°ŨÎíÏûʧšóÍųČÜŌšÖÐĩΞÓ
ĢŽŋÉđÛēėĩ―·īÓĶūįÁŌĢŽŌšÃæÉÏÓаŨÎíÐÎģÉĢŽēĒŌÝģöÓÐÆøÎķĩÄÆøĖåĢŽļÃÆøĖåŋÉĘđÕīÓÐÆ·šėĘÔŌšĩÄÂËÖ―ÍĘÉŦĄĢĮáĮáÕņĩīŨķÐÎÆŋĢŽīý°ŨÎíÏûʧšóÍųČÜŌšÖÐĩΞÓ![]() ČÜŌšĢŽÓÐēŧČÜÓÚÏĄÏõËáĩÄ°ŨÉŦģÁĩíÎöģöĄĢ
ČÜŌšĢŽÓÐēŧČÜÓÚÏĄÏõËáĩÄ°ŨÉŦģÁĩíÎöģöĄĢ
(1)ļųūÝŌÔÉÏĘĩŅéĢŽÐīģö![]() ÓëËŪ·īÓĶĩÄŧŊŅ§·―ģĖĘ―Ģš_____________________________________ĄĢ
ÓëËŪ·īÓĶĩÄŧŊŅ§·―ģĖĘ―Ģš_____________________________________ĄĢ
(2)ÕôļÉ![]() ČÜŌšĩÃēŧĩ―
ČÜŌšĩÃēŧĩ―![]() đĖĖåĢŽÖŧÄÜĩÃĩ―
đĖĖåĢŽÖŧÄÜĩÃĩ―![]() ĢŽËųŌÔđĪŌĩÉÏÍųÍųÓÃ
ĢŽËųŌÔđĪŌĩÉÏÍųÍųÓÃ![]() šÍ
šÍ![]() ŧėšÏšóđēČČĀīÖÆČĄÎÞËŪ
ŧėšÏšóđēČČĀīÖÆČĄÎÞËŪ![]() ĄĢ
ĄĢ
ĒŲÐīģöÕôļÉ![]() ČÜŌšđýģĖÖзĒÉúĩÄŧŊŅ§·īÓĶ·―ģĖĘ―__________________________________________________ĄĢ
ČÜŌšđýģĖÖзĒÉúĩÄŧŊŅ§·īÓĶ·―ģĖĘ―__________________________________________________ĄĢ
ĒÚÐīģöļÃÖÖÖÆ·ĻŋÉÐÐÐÔĩÄÔŌōĢš_______________________________________________ĢŽ_______________________________________________________________________ĄĢ(ÖÁÉŲÐīģöÁ―ļöÔŌō)ĄĢ
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋžŨ°·(CH3NH2)ĘĮŌŧÖÖŌŧÔŠČõžîĢŽÆäĩįĀë·―ģĖĘ―ÎŠĢšCH3NH2 + H2O ![]() CH3NH3+ + OHĢĄĢģĢÎÂÏÂĢŽÏō20.0 mL 0.10 mol/LĩÄžŨ°·ČÜŌšÖÐĩΞÓVmL0.10mol/LĩÄÏĄŅÎËáĢŽŧėšÏČÜŌšĩÄpHÓëÏāđØÎĒÁĢÅĻķČĩÄđØÏĩČįÍžËųĘūĄĢÏÂÁÐËĩ·ĻÖÐīíÎóĩÄĘĮ
CH3NH3+ + OHĢĄĢģĢÎÂÏÂĢŽÏō20.0 mL 0.10 mol/LĩÄžŨ°·ČÜŌšÖÐĩΞÓVmL0.10mol/LĩÄÏĄŅÎËáĢŽŧėšÏČÜŌšĩÄpHÓëÏāđØÎĒÁĢÅĻķČĩÄđØÏĩČįÍžËųĘūĄĢÏÂÁÐËĩ·ĻÖÐīíÎóĩÄĘĮ

A. bĩãķÔÓĶžÓČëŅÎËáĩÄĖåŧýV<20.00mL
B. ģĢÎÂÏÂĢŽļųūÝaĩãŋÉÖŠžŨ°·ĩÄĩįĀëÆ―šâģĢĘýKb=10 -3ĢŪ4
C. bĩãŋÉÄÜīæÔÚđØÏĩĢšc(ClĢ) > c(CH3NH3+) > c(H+) = c(OHĢ)
D. V=20.00mLĘąĢŽČÜŌšģĘČõËáÐÔ
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋÄģšÏŨũŅ§Ï°ÐĄŨéĩÄÍŽŅ§ĀûÓÃÏÂÁÐŅõŧŊŧđÔ·īÓĶÉčžÆÔĩįģØĢš2KMnO4+10FeSO4+8H2SO4ĻT2MnSO4+5Fe2ĢĻSO4ĢĐ3+K2SO4+8H2OĢŽŅÎĮÅÖÐŨ°ÓÐąĨšÍ![]() ČÜŌšĄĢÏÂÁÐÐðĘöÖÐÕýČ·ĩÄĘĮ
ČÜŌšĄĢÏÂÁÐÐðĘöÖÐÕýČ·ĩÄĘĮ

A. žŨÉÕąÖÐČÜŌšĩÄ![]() Öð―ĨžõÐĄ B. ŌŌÉÕąÖзĒÉúŧđÔ·īÓĶ
Öð―ĨžõÐĄ B. ŌŌÉÕąÖзĒÉúŧđÔ·īÓĶ
C. Íâĩį·ĩÄĩįÁũ·―ÏōĘĮīÓ![]() ĩ―
ĩ―![]() D. ĩįģØđĪŨũĘąĢŽŅÎĮÅÖÐĩÄ
D. ĩįģØđĪŨũĘąĢŽŅÎĮÅÖÐĩÄ![]() ŌÆÏōžŨÉÕą
ŌÆÏōžŨÉÕą
ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋą―ŌŌÏĐĘĮŌŧÖÖÖØŌŠĩÄŧŊđĪÔÁÏĢŽŋÉēÉÓÃŌŌą―īßŧŊÍŅĮâ·ĻÖÆąļĢŽ·īÓĶČįÏÂĢš ![]() (g)
(g)![]()
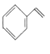 (g)+H2(g) ĄũH=+17.6kJ/molĄĢ
(g)+H2(g) ĄũH=+17.6kJ/molĄĢ
(1)īÓÎÂķČšÍŅđĮŋ―ĮķČ·ÖÎöĖáļßŌŌą―Æ―šâŨŠŧŊÂĘŋÉēÉČĄĩÄīëĘĐÓÐ___________ĄĢ
(2)đĪŌĩÉÏĢŽÍĻģĢÔÚŌŌą―ÕôÆøÖÐēôŧėËŪÕôÆø(ÔÁÏÆøÖÐŌŌą―šÍËŪÕôÆøĩÄÎïÖĘĩÄÁŋÖŪąČΊ1:4)ĢŽēâĩÃČÝÆũŨÜŅđšÍŌŌą―ŨŠŧŊÂĘËæĘąžäąäŧŊ―áđûČįÍžËųĘūĄĢ

ĒŲēôČëËŪÕôÆøÄÜĖáļßŌŌą―ĩÄÆ―šâŨŠŧŊÂĘĢŽ―âĘÍËĩÃũļÃĘÂĘĩ__________ĄĢ
Æ―šâģĢĘýKp=_______kPa(KpΊŌÔ·ÖŅđąíĘūĩÄÆ―šâģĢĘý)
ĒÚ·īÓĶËŲÂĘV=VÕý-VÄæ=kÕýPŌŌą―-kÄæpą―ŌŌÏĐpĮâÆøĢŽkÕýĄĒkÄæ·ÖąðΊÕýÄæ·īÓĶËŲÂĘģĢĘýĄĢžÆËãaīĶĩÄ![]() ______ĄĢ
______ĄĢ
(3)CO2Æø·ÕÏÂŌŌą―īßŧŊÍŅĮâŋÉÍŽĘąīæÔÚÍž1Á―ÖÖÍūūķĢš

ĒŲb=_______kJ/molĄĢ
ĒÚÍūūķIĩÄ·īÓĶĀúģĖÍžËųĘūĢŽÏÂÁÐËĩ·ĻÕýČ·ĩÄĘĮ______________ĄĢ
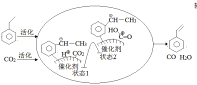
aĢŪCO2ΊŅõŧŊžÁ
bĢŪŨīĖŽ1ĩ―ŨīĖŽ2ÐÎģÉÁËO-Hžü
cĢŪÖОäēúÎïÖŧÓÐ(![]() )
)
dĢŪļÃīßŧŊžÁŋÉĖáļßŌŌą―ĩÄÆ―šâŨŠŧŊÂĘ
ĒÛÔÚÏāÍŽĩÄČÝÆũÖÐĢŽēŧÍŽp(CO2)ĩÄĖõžþÏÂĢŽ―øÐÐÏāÍŽĩÄ·īÓĶĘąžäĢŽp(CO2)ÓëŌŌą―ŨŠŧŊÂĘđØÏĩČįÍžĢŽ·ÖÎöĢŽp(CO2)Ί15kPaĘąŌŌą―ŨŠŧŊÂĘŨîļßĩÄŌō____________________ĄĢ

ēéŋīīð°ļšÍ―âÎö>>
ŋÆÄŋĢšļßÖÐŧŊŅ§ ĀīÔīĢš ĖâÐÍĢš
ĄūĖâÄŋĄŋÏÂÁÐĘĩŅéēŧÄÜīïĩ―ÔĪÆÚÄŋĩÄĘĮ
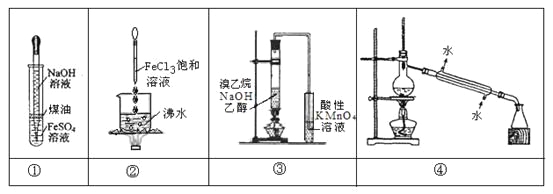
A.ĘĩŅéĒŲĢšž·ģö―šÍ·ĩÎđÜÖÐĩÄNaOHČÜŌšĢŽđÛēėFe(OH)2ģÁĩíĩÄŅÕÉŦ
B.ĘĩŅéĒÚĢšžĖÐøÖó·ÐČÜŌšÖÁšėšÖÉŦĢŽÍĢÖđžÓČČĢŽĩąđâĘøÍĻđýĖåÏĩĘąēúÉúķĄīïķûЧÓĶ
C.ĘĩŅéĒÛĢšÍĻđýđÛēėËáÐÔKMnO4ČÜŌšŨÏÉŦÍĘČĨĢŽČ·ČÏÓÐŌŌÏĐÉúģÉ
D.ĘĩŅéĒÜĢšŋØÖÆŌŧķĻÎÂķČĢŽ―ŦĘŊÓÍ·ÖĀëΊÆûÓÍĄĒēņÓÍĩČ
ēéŋīīð°ļšÍ―âÎö>>
°ŲķČÖÂÐÅ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com