
【题目】写出下对反应的化学方程式,并注明反应类型:
(1)乙醇制乙烯:__,反应类型:__。
(2)乙醇与浓氢溴酸反应:__,反应类型__。
(3)苯酚与浓溴水反应:__,反应类型__。
(4)乙醛与新制氢氧化铜悬浊液反应:__,反应类型__。
【答案】CH3—CH2OH![]() CH2=CH2↑+H2O 消去反应 CH3CH2OH+HBr
CH2=CH2↑+H2O 消去反应 CH3CH2OH+HBr![]() CH3—CH2—Br+H2O 取代反应
CH3—CH2—Br+H2O 取代反应 ![]() +3Br2
+3Br2 ↓+3HBr 取代反应 CH3CHO+NaOH+2Cu(OH)2
↓+3HBr 取代反应 CH3CHO+NaOH+2Cu(OH)2![]() CH3COONa+Cu2O↓+3H2O 氧化反应
CH3COONa+Cu2O↓+3H2O 氧化反应
【解析】
(1)乙醇和浓硫酸混合加热至170℃,发生消去反应得到乙烯:CH3—CH2OH![]() CH2=CH2↑+H2O。
CH2=CH2↑+H2O。
(2)乙醇与浓氢溴酸共热,发生取代反应,生成溴乙烷和水:CH3CH2OH+HBr![]() CH3—CH2—Br+H2O。
CH3—CH2—Br+H2O。
(3)苯酚与浓溴水混合,发生取代反应,苯环上和连接羟基的碳原子处于邻对位的碳原子上的氢原子被溴原子取代,生成三溴苯酚白色沉淀:![]() +3Br2
+3Br2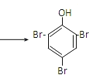 ↓+3HBr。
↓+3HBr。
(4)乙醛与新制氢氧化铜悬浊液共热,乙醛被氧化,在碱性溶液中生成乙酸盐,同时生成红色沉淀氧化亚铜:CH3CHO+NaOH+2Cu(OH)2![]() CH3COONa+Cu2O↓+3H2O。
CH3COONa+Cu2O↓+3H2O。


科目:高中化学 来源: 题型:
【题目】已知:①(![]() +HNO3
+HNO3![]()
![]() +H2O △H<0;②硝基苯沸点210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是
+H2O △H<0;②硝基苯沸点210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持仪器略去),正确的是
选项 | A | B | C | D |
装置 |
|
|
|
|
目的 | 分液 | 配制混酸 | 水浴加热 | 蒸馏提纯 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨硼烷(NH3BH3)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)H、B、N中,原子半径最大的是______。根据对角线规则,B的一些化学性质与元素______的相似。
(2)NH3BH3分子中,N—B化学键称为____键,其电子对由____提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH3+![]() +9H2,
+9H2,![]() 的结构如图所示:
的结构如图所示: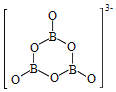 ;在该反应中,B原子的杂化轨道类型由______变为______。
;在该反应中,B原子的杂化轨道类型由______变为______。
(3)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是__________。与NH3BH3原子总数相等的等电子体是_________(写分子式),其熔点比NH3BH3____________(填“高”或“低”),原因是在NH3BH3分子之间,存在____________________,也称“双氢键”。
(4)研究发现,氦硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
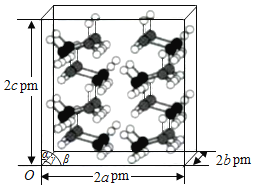
氨硼烷晶体的密度ρ=___________g·cm3(列出计算式,设NA为阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
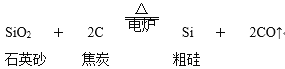
【题目】从硅的氧化物可以制取硅单质,主要化学反应如下:粗硅的制取:
由粗硅制纯硅(常用方法):Si(粗)+2Cl2![]() SiCl4 SiCl4+2H2
SiCl4 SiCl4+2H2![]() Si(纯)+4HCl
Si(纯)+4HCl
根据以上反应,回答下列问题。
(1)在制取粗硅的反应中,焦炭的作用是什么___?
(2)在由粗硅制纯硅的反应中,氯气(Cl2)与Si的反应属于什么类型的反应___?SiCl4与H2的反应属于什么类型的反应___?H2的作用是什么___?
(3)在半导体工业中有这样一句行话:“从沙滩到用户”,你是如何理解的___?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是制取SO2并验证SO2某些性质的装置图。
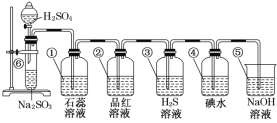
试回答:
(1)⑥中发生反应的化学方程式为___。
(2)①中的实验现象为___,此实验证明SO2是___氧化物。
(3)②中的品红溶液___,证明SO2有___。
(4)③中的H2S溶液____,证明SO2有___。
(5)④中的碘水___,证明SO2有____。
(6)⑤中NaOH溶液的作用是___,有关反应的化学方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.丙烯的结构简式为CH2CHCH3
B.分子式为C4H10O属于醇类的有机物有4种
C.分子式为C2H4O2和C3H6O2的有机物一定互为同系物
D.![]() 名称为丙酸甲酯
名称为丙酸甲酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以确保化学实验的绿色化。
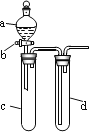
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是_____________________________________________________________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL的浓硝酸。反应一段时间后,再由a向c中加2 mL蒸馏水,c中的实验现象有什么变化___________。
方案 | 甲 | 乙 | 丙 |
反应物 | Cu、浓HNO3 | Cu、稀HNO3 | Cu、O2、稀HNO3 |
(3)如表所示是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是__________,理由是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成一种用于合成 γ 分泌调节剂的药物中间体,其合成的关键一步如图。下列有关化合物甲、乙的说法正确的是

A.甲→乙的反应为加成反应
B.甲分子中至少有 8 个碳原子在同一平面上
C.甲、乙均不能使溴水褪色
D.乙与足量 H2 完全加成的产物分子中含有 4 个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素![]() 在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是
在元素周期表中的相对位置如图所示,其中w原子的最外层电子数是最内层电子数的3倍.下列判断不正确的是![]()

A.x与同主族且相邻元素的气态氢化物的沸点,前者高于后者
B.含Y元素的盐溶液有的显酸性,有的显碱性
C.x的气态氢化物与w的最高价氧化物的水化物反应只能生成一种盐
D.x与H、O元素形成的化合物可以组成一种盐,其中![]() 元素原子个数之比为2:4:3
元素原子个数之比为2:4:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com