
| A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
| B.除去Cl2中的少量HCl:通入饱和食盐水,干燥后收集气体 |
| C.除去NaCl溶液中少量CaCl2:加入适量Na2CO3,过滤 |
| D.除去KCl溶液中少量MgCl2:加入适量NaOH溶液,过滤 |
科目:高中化学 来源:不详 题型:单选题
A. 用CCl4提取溴水中的Br2 |
B. 除去乙醇中的甲醇 |
C. 从KI和I2的固体混合物中回收I2 |
D. 配制100mL 0.1000mol?L-1 K2Cr2O7溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 物质 | 检验试剂 | 除杂试剂 |
| 甲烷(乙烯) | ______ | ______ |
| 酒精(水) | ______ | ______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲烷中的甲醛(水,洗气) |
| B.乙烷中的乙烯(酸性高锰酸钾溶液,洗气) |
| C.乙酸乙酯中的乙酸(NaOH溶液,分液) |
| D.苯中的苯酚(浓Br2水,过滤) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| C.除去NaHCO3溶液中Na2CO3:加适量稀盐酸 |
| D.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2?H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |

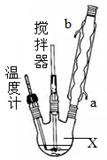
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制乙酸乙酯时,迅速将乙醇注入浓硫酸中 |
| B.在石油蒸馏装置中,将温度计水银球插入液面以下 |
| C.用铂丝蘸取少量KCl溶液置于火焰上灼烧,直接观察火焰颜色,检验K+的存在 |
| D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com