
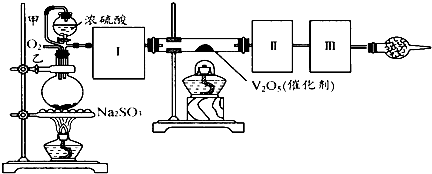

���� ��1��������Ũ��������������������壻SO3���۵���16��8�棬�ϵͣ������ñ�ˮ����������������ü�ʯ�һ�������������Һ����β��������
��2���ȼ��ȴ����ٵ���Ũ���ᣬ�ܱ�֤�����Ķ��������ܶ��ת��Ϊ��������
��3��������������ԣ�������Ԫ�صĻ��ϼ�Ϊ+5�ۣ�����ת�Ƶĵ��������жϲ�������Ԫ�صļ�̬��
��4��������ԭ���غ����ȷ�����������ת���ʣ�
��5�������е�CO2��ˮ��������ŲⶨSO2ת����SO3��ת���ʣ�
��� �⣺��1����װ�ñ���Ҫ�Զ���������и��������Ũ��������������������壻SO3���۵���16��8�棬�����ñ�ˮ�������������δ��Ӧ���Ķ�������Կ����������Ⱦ�������ü�ʯ�һ�������������Һ������β��������
�ʴ�Ϊ��B�� A��E����C����
��2��Ϊ��֤�����Ķ��������ܶ��ת��Ϊ��������Ӧ�ȼ��ȴ����ٵ���Ũ���ᣬ
�ʴ�Ϊ���ȼ��ȴ����ٵ���Ũ���
��3��������������ԣ�������Ԫ�صĻ��ϼ�Ϊ+5�ۣ���1.5��6.02��1023����1.5mol����ת��ʱ��1.5mol��������Ԫ�صĻ��ϼ�Ӧ��+5�۽���+4�ۣ����Բ�������Ԫ���Զ������ȵ���ʽ���ڣ�������������Ϊ���ᣬ
�ʴ�Ϊ��SO2+2HClO3=H2SO4+2ClO2��
��4��������ԭ���غ㣬Na2SO3��SO2��SO3��amolNa2SO3��ĩ������Ũ������д�ʵ�飬����Ӧ����ʱ��Ӧ�����������������Ϊ64ag�����װ�â�������bg����Ϊʣ�������������������Զ��������ת���ʦ�=$\frac{64a-b}{64}$��100%=$\frac{1600a-25b}{16a}$%��
�ʴ�Ϊ��$\frac{1600a-25b}{16a}$��
��5�������е�CO2��ˮ��������ŲⶨSO2ת����SO3��ת���ʣ�����Ҫ��һ������װ�ã�
�ʴ�Ϊ����ֹ�����е�CO2��ˮ�������ţ������
���� ������Ҫ�����˶�����������ʡ������Լ����ӵļ����֪ʶ���ۺ��Խ�ǿ����Ŀ�Ѷ��еȣ�����ѧ�������ͽ�������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
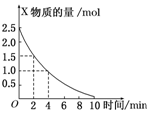 ���ݻ�Ϊ3L���ܱ������У�������̬����X��Y��һ�������·�����Ӧ2X+Y�T2Z����ͼ��ʾ�Ǹ÷�Ӧ��X�����ʵ�����ʱ��仯�����ߣ�
���ݻ�Ϊ3L���ܱ������У�������̬����X��Y��һ�������·�����Ӧ2X+Y�T2Z����ͼ��ʾ�Ǹ÷�Ӧ��X�����ʵ�����ʱ��仯�����ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ָ����� | B�� | �ڻ�ҩ��ը��������ԭ��Ӧ | ||
| C�� | ��Ӧ���Ȳ������������� | D�� | ľ̿�ڷ�Ӧ�б���ԭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe��FeSO4 | B�� | Cu��NO3��2��Cu | C�� | CO��CO2 | D�� | NaCl��AgCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ͭ�����ʵ�����ͬ | |
| B�� | Ũ���������������� | |
| C�� | ϡ���ᱻ��ԭ֮���������ļ�̬���ͣ�����ϡ����������Ը�ǿ | |
| D�� | ������Ӧ�еĵ���ת�Ƶ���Ŀ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
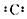 B-�Ľṹʾ��ͼ
B-�Ľṹʾ��ͼ C+�ĵ���ʽNa+
C+�ĵ���ʽNa+�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com